Sốt xuất huyết do sốt xuất huyết Arenavirus: mầm bệnh gây chết người và ức chế miễn dịch tiềm tàng.CHUYEN NGU TIENG ANH SANG TIENG VIET=THICH NU CHAN TANH.
- 1Chương trình sau đại học về sinh hóa, sinh học phân tử và sinh lý học, Đại học sốt thất thường (HF) do nhiễm arenavirus gây bệnh truyền thống đã bị bỏ qua vì các bệnh nhiệt đới ảnh hưởng chủ yếu đến các khu vực châu Phi và Nam Mỹ. Hiện tại không có vắc-xin được FDA chấp thuận cho arenavirus, và các phương pháp điều trị đã bị giới hạn trong liệu pháp hỗ trợ và sử dụng các chất tương tự nucleoside không đặc hiệu, như Ribavirin. Sự bùng phát của nhiễm trùng arenavirus đã được giới hạn ở một số khu vực địa lý nhất định là các trường hợp xuất khẩu arenavirus từ các vùng lưu hành và những thách thức kinh tế xã hội đối với việc kiểm soát các ổ chuột gặm nhấm gây lo ngại nghiêm trọng về khả năng bùng phát trong tương lai. Tổng quan này tổng hợp kiến thức hiện tại về sự tiến hóa của arenavirus, hệ sinh thái, mô hình truyền bệnh,
Giới thiệu
Những tiến bộ đáng kể đã được thực hiện trong những năm gần đây để hiểu được vai trò của các phương tiện du lịch hiện đại trong việc vô tình xuất khẩu các arenavirus gây chết người từ các vùng lưu hành, sinh học cơ bản của các virut này, tiến hóa gen và phương thức lây truyền và ức chế miễn dịch của chúng. họ rất có trách nhiệm. Một mức độ hiểu biết chi tiết về vòng đời của virus, sự tiến hóa và tương tác với các con đường truyền tín hiệu miễn dịch của vật chủ là cần thiết để thiết kế các biện pháp phòng ngừa và điều trị hiệu quả chống lại nhóm mầm bệnh chết người này.
Phân loại, tiến hóa và sinh thái Arenavirus
Họ Arenaviridae được chia thành 3 chi dựa trên vật chủ tự nhiên của họ là Mam Mamenenirire, Reptarenaviridae và Hartmaniviridae , bao gồm virut lây nhiễm ở động vật có vú, bò sát và cá, tương ứng ( 1 , 2 ). Mammarenaviridae được chia thành các khu vực có nguồn gốc của họ, chẳng hạn như Cựu Thế giới (OW) virus tìm thấy ở Tây Phi ( 3 - 9 ) và (NW) virus New World tìm thấy ở Nam Mỹ ( 5 , 10 - 17 ), trong đó được cho là có nguồn gốc <23.000 và 41.000 năm trước tại các lục địa này, tương ứng ( 18 ) (Hình 1 ). Ngoài ra, một số chủng vi rút arenavirus đã được phát hiện ở Hoa Kỳ, được nghi ngờ có khả năng gây bệnh cho người ( 19 , 20 ). Các phân nhóm OW và NW là đa chủng và chứa cả các chủng virus gây bệnh ở người và không gây bệnh, với tổng số 10 chủng được biết là gây bệnh cho người ( 21 ). Không giống như các loại virus sốt xuất huyết khác, chẳng hạn như virus Ebola (EBOV), việc truyền arenavirus sang người đã được tìm thấy chủ yếu do sự tương tác của con người với các loài gặm nhấm như là nguồn dự trữ tự nhiên của các loại virus này, như đã được quan sát trực tiếp gần đây vào năm 2017 Sự bùng phát virus Lass2018 ở Nigeria ( 9). Tuy nhiên, lây truyền từ người sang người có thể đóng một vai trò lớn hơn trong một số đợt bùng phát virus nhất định, chẳng hạn như đợt bùng phát năm 2014, nơi các chủng trên các khu vực địa lý lớn hơn được tìm thấy tập trung lại gần nhau ( 22 ).
Hình 1 . Phân loại và vị trí của arenaviruses. Cây phát sinh gen cho các chủng arenavirus OW và NW và vị trí địa lý của chúng. Cây được tạo ra từ các chuỗi gen dài toàn phần cho protein L polymerase được căn chỉnh theo phân tích Clustalw. Dấu hoa thị chỉ định các chủng gây bệnh tự nhiên ở người, trong khi hashtags chỉ định các chủng có thể gây bệnh trong phòng thí nghiệm ở động vật.
Mô hình truyền bệnh này đưa ra một thách thức thú vị để xác định lịch sử tiến hóa của arenaviruses. Cũng như nhiều loại virut gây bệnh theo mô hình đồng phân để cho phép lây nhiễm vật chủ mới, arenavirus trước đây được cho là có nguồn gốc ở châu Á cùng với các loài gặm nhấm sớm nhất và sau đó lan sang châu Âu, châu Phi và châu Mỹ cùng với sự lây lan của các loài gặm nhấm ( 23 , 24 ). Tuy nhiên, cây phát sinh vật chủ arenavirus và loài gặm nhấm hầu như không bao giờ khớp hoàn hảo ( 25 ) và một số mô hình dẫn đến vật chủ của loài gặm nhấm được tích hợp ngẫu nhiên vào bộ phát sinh arenavirus ( 26 ). Ngoài ra, chỉ có vi rút viêm màng phổi lympho (LCMV) được tìm thấy lưu hành giữa các loài gặm nhấm châu Âu (18 , 27 - 30 ), nhưng các chất chuẩn độ chống lại LCMV đã được tìm thấy ở các đối tượng người trên toàn thế giới ( 31 , 32 ), cho thấy rằng loài gặm nhấm và các vật chủ khác có khả năng cho LCMV phổ biến hơn so với suy nghĩ trước đây. Các nghiên cứu gần đây đã tiết lộ rằng LCMV có thể được phân lập từ bọ ve ở Ukraine ( 33 ) và ở Trung Quốc ( 34 ) (mặc dù số lượng mẫu bệnh phẩm bị nhiễm dương tính thấp và khả năng LCMV chưa biết để lây nhiễm tế bào côn trùng làm cho một số nghi ngờ về bọ ve là sự thật hồ chứa chứ không phải là một chất mang virus không liên tục). Do đó, sự tiến hóa của Arenavirus có thể phản ánh rõ hơn sự thích nghi của chúng với các vật chủ có sẵn dựa trên các hạn chế về địa lý ( 9 , 18 ).
Sự thích nghi của vật chủ địa phương đối với arenaviruses được chứng minh rõ hơn bởi những hiểu biết gần đây về sự đa dạng của arenavirus ở các loài bò sát và vật chủ biển. Trình tự bộ gen đầy đủ đã được xác định đối với ba loại virus reptarenav phân lập từ boa constrictor và boa cây được xác định: virus CAS ( 35 ), virus Golden Gate ( 35 ) và virus Đại học Helsinki ( 36 ), cần phải thêm chi Reptarenaviridae vào Họ Arenaviridae năm 2015 ( 1 ). Ba loại reptarenavirus này đã được tìm thấy là tác nhân gây bệnh bao gồm bệnh cơ thể bao gồm (IBD), một tình trạng gây tử vong ở rắn đặc trưng bởi các bất thường về thần kinh ( 37 , 38), Quy tụ eosinophilic lớn bên trong các tế bào bị nhiễm ( 37 - 40 ) bao gồm một protein 68 kDa ( 39 ) được cho là nucleoproteins reptarenaviral (NP) ( 36 , 41 ) và là nguồn chủ yếu của nhiễm trùng thứ phát gây chết là ( 38 - 40 ). Bằng chứng sơ bộ đã chỉ ra rằng reptarenavirus có thể thích nghi đặc biệt với các yếu tố boa, với sự nhân lên của virus là tối ưu ở bò sát 30 ° C và bị suy giảm khi được nuôi ở điều kiện động vật có vú 37 ° C ( 41 ) và các vi khuẩn boa bị nhiễm bệnh đã giảm tỷ lệ IBD và tăng cơ hội trở thành người mang virus không triệu chứng so với các loài rắn khác mặc dù tải lượng virus cao (37 , 38 , 42 ). Giống như các bể chứa động vật gặm nhấm, reptarenavirus cũng đã được tìm thấy để truyền theo chiều dọc ( 43 ). Trong khi đó, bộ gen của mammarenavirus được phân chia hai phần với phân đoạn nhỏ (S) và phân đoạn (L) lớn, những loài reptarenavirus có khả năng phức tạp hơn, với một số loài rắn bị nhiễm bệnh mang đến 4 phân đoạn S khác nhau và 11 phân đoạn L khác nhau mỗi cá nhân ( 44 ). Thêm vào sự đa dạng bộ gen của arenavirus là phát hiện gần đây về hai loại arenavirus mới lây nhiễm cá vây vây ( 2 ) với bộ gen ba đoạn, làm cho chúng trở thành một trung gian tiềm năng giữa arenaviruses và virut Bunyaviridae gần gũi của chúng, gia đình được tìm thấy rộng rãi trong động vật chân đốt ( 2 , 45 ) cũng có thể gây nhiễm trùng xuất huyết nghiêm trọng và gây tử vong ở người.
Trọng tâm của bài viết này là về các mammarenavirus của OW và NW. Về mặt phát sinh, những thay đổi trong polymerase của virut mammarenavirus có thể liên quan nhiều hơn đến các sự kiện thích nghi cũ có liên quan đến sự đặc tả của NW arenaviruses ( 18 ), trong khi sự thích nghi hiện tại, ít nhất là với virus OW Lassa (LASV), dường như nổi bật hơn với glycoprotein bề mặt virus ( 46 ). Quan sát này được tóm tắt lại khi so sánh sự giống nhau về di truyền của bốn protein arenavirus ( Hình 2). Các polymerase arenavirus có ít tương đồng giữa các virus OW và NW cũng như giữa các chủng OW và NW so với 3 protein arenavirus khác, cho thấy sự khác biệt di truyền sớm hơn. Một báo cáo gần đây hỗ trợ thêm cho quan sát này bằng cách lưu ý rằng một loại virut được sắp xếp lại có chứa đoạn gen S mã hóa glycoprotein của virus (GP) và nucleoprotein (NP) từ LASV Josiah và đoạn genome L đã mã hóa virus polymerase (L) và protein ma trận (Z) từ chủng Liberia LASV ít độc lực được biết đến năm 2015 vẫn giữ được khả năng gây bệnh ở lợn guinea ( Hình 3 ). Ngược lại, một loại virut tái tổ hợp khác mang GP virus và NP từ chủng Liberia 2015 đã bị suy giảm nghiêm trọng ( 47). Kết hợp lại với nhau, điều này cho thấy rằng việc thích nghi trước với vật chủ có sẵn về mặt địa lý đòi hỏi phải có những thay đổi cơ bản đối với các protein virut bên trong, như L polymerase, trong khi sự tiến hóa gần đây được thúc đẩy bằng cách tối ưu hóa hiệu quả xâm nhập của virus và sự trốn tránh miễn dịch qua trung gian GP và NP . Khái niệm về protein virut làm trung gian cho sự trốn tránh miễn dịch của vật chủ sẽ được thảo luận thêm dưới đây.
Hình 2 . L RdRp polymerase thể hiện sự bảo tồn ít nhất trong số các protein arenavirus. Các trình tự mã hóa protein có độ dài đầy đủ từ các chủng arenavirus được căn chỉnh theo phân tích Clustlw và ma trận cho độ tương tự điểm số theo cặp (số dư lượng axit amin chia sẻ / độ dài liên kết * 100) đã được chuyển đổi thành sơ đồ nhiệt cho mô đun pheatmap cho R. ID gia nhập của GenBank được sử dụng để sắp xếp trong Hình 1 , 2 như sau: NC_010249 (Allpahuayo L), NC_010253 (Allpahuayo S), NC_010251.1 (Amapari L), NC_010247 (Amapari S), NC_010255 (Bear Canyon L), NC_010256 (Bear Canyon L), NC_010256 (Bear Canyon L) JQ717262 (CAS S), NC_010563 (Chapare L), NC_010562 (Chapare S), NC_010252 (Cupixi L), NC_010254 (Cupixi S), NC_010759 (Flexal L), NC_010757 (Flexal S), NC7 (Golden Gate S), NC_005082 (Guanarito L), NC_005077 (Guanarito S), NC_007906 (Ippy L), NC_007905 (Ippy S), NC_005080 (Junin L), NC_005081 (Junin S), HQ68888 (L vật , NC_010760 (Latino L), NC_010758 (Latino S), AY847351 (LCMV L), AY847350 (LCMV S), NC_012777 (Lujo L),NC_012776 (Lujo S), NC_005079 (Machupo L), NC_005078 (Machupo S), NC_007904 (Mobala L), NC_007903 (Mobala S), NC_006574 (Mopeia L), NC_006575 (Mopeia L), NC_006575 (Mopeia L) Olivero S), NC_010761 (Parana L), NC_010756 (Parana S), NC_006439 (Pichinde L), NC_006447 (Pichinde S), NC_005897 (Pirital L), NC_005894 (Pirital S), NC_00589 ), NC_004292 (Tacaribe L), NC_004293 (Tacaribe S), NC_010702 (Tamiami L), NC_010701 (Tamiami S), KF297880 (Đại học Helsinki S), KF297881 (Đại học Helsinki L), MG5 MG599864 (Wenling ếchfish 1 S), MG59986 (Wenling ếchfish 1 M), MG599866 (Wenling ếchfish 2 L), MG599867 (Wenling Frogfish 2 S), MG599868 (Wenling Frogfish 2 M), NC_010703 (Whitling Arroyo S).NC_005078 (Machupo S), NC_007904 (Mobala L), NC_007903 (Mobala S), NC_006574 (Mopeia L), NC_006575 (Mopeia S), NC_010250 (Olivero L), NC_010248 (Oliver Parana S), NC_006439 (Pichinde L), NC_006447 (Pichinde S), NC_005897 (Pirital L), NC_005894 (Pirital S), NC_006313 (Sabia L), NC_006317 (Sabia S), NC42 ), NC_010702 (Tamiami L), NC_010701 (Tamiami S), KF297880 (Đại học Helsinki S), KF297881 (Đại học Helsinki L), MG599863 (Cá ếch ếch 1 L), MG599864 (Cá ếch 1) 1 M), MG599866 (Wenling ếchfish 2 L), MG599867 (Wenling ếchfish 2 S), MG599868 (Wenling ếchfish 2 M), NC_010703 (Whitewater Arroyo L), NC_010700 (Whitewater Arroyo S).NC_005078 (Machupo S), NC_007904 (Mobala L), NC_007903 (Mobala S), NC_006574 (Mopeia L), NC_006575 (Mopeia S), NC_010250 (Olivero L), NC_010248 (Oliver Parana S), NC_006439 (Pichinde L), NC_006447 (Pichinde S), NC_005897 (Pirital L), NC_005894 (Pirital S), NC_006313 (Sabia L), NC_006317 (Sabia S), NC42 ), NC_010702 (Tamiami L), NC_010701 (Tamiami S), KF297880 (Đại học Helsinki S), KF297881 (Đại học Helsinki L), MG599863 (Cá ếch ếch 1 L), MG599864 (Cá ếch 1) 1 M), MG599866 (Cá ếch Wenling 2 L), MG599867 (Cá ếch Wenling 2 S), MG599868 (Cá ếch Wenling 2 M), NC_010703 (Whitewater Arroyo L), NC_010700 (Whitewater Arroyo S).NC_006575 (Mopeia S), NC_010250 (Olivero L), NC_010248 (Olivero S), NC_010761 (Parana L), NC_010756 (Parana S), NC_006439 (Pichinde L), NC_006447 (Pichinde L), NC_006447 (Pichinde L) Pirital S), NC_006313 (Sabia L), NC_006317 (Sabia S), NC_004292 (Tacaribe L), NC_004293 (Tacaribe S), NC_010702 (Tamiami L), NC_010701 (Tamiami S), K29 Đại học Helsinki L), MG599863 (Wenling ếchfish 1 L), MG599864 (Wenling ếchfish 1 S), MG59986 (Wenling ếchfish 1 M), MG599866 (Wenling Frogfish 2 L), MG599867 (Wenling Frogfish 2 S) 2 M), NC_010703 (Whitwater Arroyo L), NC_010700 (Whitwater Arroyo S).NC_006575 (Mopeia S), NC_010250 (Olivero L), NC_010248 (Olivero S), NC_010761 (Parana L), NC_010756 (Parana S), NC_006439 (Pichinde L), NC_006447 (Pichinde L), NC_006447 (Pichinde L) Pirital S), NC_006313 (Sabia L), NC_006317 (Sabia S), NC_004292 (Tacaribe L), NC_004293 (Tacaribe S), NC_010702 (Tamiami L), NC_010701 (Tamiami S), K29 Đại học Helsinki L), MG599863 (Wenling ếchfish 1 L), MG599864 (Wenling ếchfish 1 S), MG59986 (Wenling ếchfish 1 M), MG599866 (Wenling Frogfish 2 L), MG599867 (Wenling Frogfish 2 S) 2 M), NC_010703 (Whitwater Arroyo L), NC_010700 (Whitwater Arroyo S).NC_005894 (Pirital S), NC_006313 (Sabia L), NC_006317 (Sabia S), NC_004292 (Tacaribe L), NC_004293 (Tacaribe S), NC_010702 (Tamiami L), NC_010701 (Tamiami L) KF297881 (Đại học Helsinki L), MG599863 (Wenling ếchfish 1 L), MG599864 (Wenling ếchfish 1 S), MG59986 (Wenling Frogfish 1 M), MG599866 (Wenling Frogfish 2 L), MG599867 (Wenling Cá ếch vằn 2 M), NC_010703 (Whitwater Arroyo L), NC_010700 (Whitwater Arroyo S).NC_005894 (Pirital S), NC_006313 (Sabia L), NC_006317 (Sabia S), NC_004292 (Tacaribe L), NC_004293 (Tacaribe S), NC_010702 (Tamiami L), NC_010701 (Tamiami L) KF297881 (Đại học Helsinki L), MG599863 (Wenling ếchfish 1 L), MG599864 (Wenling ếchfish 1 S), MG59986 (Wenling Frogfish 1 M), MG599866 (Wenling Frogfish 2 L), MG599867 (Wenling Cá ếch vằn 2 M), NC_010703 (Whitwater Arroyo L), NC_010700 (Whitwater Arroyo S).MG599867 (Wenling ếchfish 2 S), MG599868 (Wenling ếchfish 2 M), NC_010703 (Whitwater Arroyo L), NC_010700 (Whitewater Arroyo S).MG599867 (Wenling ếchfish 2 S), MG599868 (Wenling ếchfish 2 M), NC_010703 (Whitwater Arroyo L), NC_010700 (Whitewater Arroyo S).
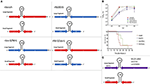
Hình 3 . Đoạn S của bộ gen virus Lass là đủ để duy trì khả năng gây bệnh. (A) Sử dụng chiến lược di truyền ngược để tạo ra các loại virut dại tái tổ hợp (WT) và tái tổ hợp các virut Lass mang các phân đoạn lớn (L) và nhỏ (S) khác nhau từ các chủng virut khác nhau (Josiah so với NJ2015). Các gen virut: ma trận Z, L RdRp, glycoprotein (GP) và nucleoprotein (NP); IGR, khu vực giữa các thế hệ. (B) Động học tăng trưởng của các virus được liệt kê trong 2A trong các tế bào A549 và đường cong sống sót của chủng chuột lang 13 / N tiêm dưới da bị nhiễm các virus này. Hình vẽ lại từ Welch et al. ( 47 ). (C) Minh họa về hàm lượng gen của vắc-xin ứng cử viên ML29 LASV mang phân đoạn L từ vi-rút Mopeia (MOPV) và phân đoạn S từ LASV.
Truyền bệnh và ý nghĩa xã hội
Mammarenavirus xâm nhập vào vật chủ của chúng bằng cách hít phải các hạt virus gây ra trong không khí hoặc bằng cách ăn và / hoặc uống thực phẩm hoặc nước bị nhiễm virus. Các cấu trúc xã hội của các vùng lưu hành arenavirus đưa ra một thách thức đặc biệt đối với việc ngăn chặn virus với mô hình lây truyền này. Các ngôi nhà thường là không gian ngoài trời và chứa không gian nhỏ để chuột sống chung với con người khi được xây dựng từ các vật liệu có sẵn tại địa phương. Do đó, các hồ chứa động vật gặm nhấm di chuyển dễ dàng từ nhà này sang nhà khác ( 48 ) và các cuộc khảo sát trước đây đã tìm thấy một số lượng đáng kể các ngôi nhà có chứa các loài gặm nhấm và các trường hợp tiếp xúc với các sản phẩm chất thải của loài gặm nhấm hoặc gặm nhấm, đặc biệt là vào ban đêm khi hoạt động của loài gặm nhấm ở mức cao nhất cấp độ ( 49). Lúa thường là cây trồng ổn định ở các khu vực lưu hành (đặc biệt là ở phía tây châu Phi), thường được trồng trên các cánh đồng hoặc đầm lầy thấp khuyến khích nơi cư trú của loài gặm nhấm ( 50 ). Những thách thức do cơ sở hạ tầng giáo dục và truyền thông ở các vùng lưu hành cũng ngăn chặn việc kiểm soát dịch bệnh tối ưu, với một cuộc khảo sát gần đây cho thấy 76% cư dân ở một thị trấn ở Nigeria có kiến thức không đầy đủ về bệnh sốt Lass và 51% có các biện pháp kiểm soát kém ( 51 ). Các thực hành như săn bắt chuột để lấy thức ăn và sử dụng trong các nghi lễ hiến tế cũng đã được ghi nhận để tăng nguy cơ nhiễm trùng ( 50). Các biện pháp phòng chống dịch bệnh trong tương lai sẽ không chỉ cần tập trung vào việc thực thi các thói quen kiểm soát gặm nhấm cá nhân mà còn khuyến khích các chính sách khuyến khích và chính trị lớn hơn có lợi cho việc nuôi dưỡng các thói quen hợp lý ( 52 , 53 ) và xây dựng cơ sở hạ tầng, vì phòng thí nghiệm chẩn đoán có khả năng thực hiện virus. PCR genomic để phát hiện nhiễm trùng arenavirus thường không có sẵn ở các vùng lưu hành ( 54 - 56 ). Mô hình tính toán của các khu vực có nguy cơ xảy ra đại dịch arenavirus cũng sẽ tiếp tục là cần thiết như các biện pháp dự đoán / phòng ngừa ( 53 , 57 - 60 ).
Một số nghiên cứu mô hình đã chỉ ra rằng một số khu vực châu Phi gần với các khu vực lưu hành hiện tại có nguy cơ lây lan arenavirus nghiêm trọng ( 53 , 57 , 58 ) và các hồ chứa mới cho arenavirus gây bệnh ở người đang tiếp tục được tìm thấy, làm tăng thêm tiềm năng cho liên vùng lây lan ( 61 ). Tuy nhiên, yếu tố lớn nhất trong việc hạn chế đại dịch arenavirus dường như là một rào cản lây truyền ký chủ giữa các loài mạnh mẽ ( 62 ). Các mô hình hiện tại cho thấy khoảng 10% số loài gặm nhấm ở các khu vực lưu hành là huyết thanh dương tính với arenavirus tại địa phương và loài gặm nhấm này loại bỏ virus trong một khoảng thời gian ngắn hơn đáng kể so với tuổi thọ của chúng để tạo ra kháng thể ( 63 , 64) với một số bằng chứng sơ bộ cho thấy rằng các kháng thể chống arenavirus có thể có một mối tương quan nhỏ với giảm tỷ lệ sống sót và tăng sự bắt giữ của loài gặm nhấm ( 65 ).
Ngày càng có nhiều lo ngại về khả năng arenavirus lan rộng khắp các khu vực và khởi đầu các đại dịch trên toàn thế giới. LASV vẫn là loại arenavirus được ghi nhận duy nhất được nhập khẩu bởi những khách du lịch đã đến thăm các vùng đặc hữu vì nhiều lý do ( Bảng bổ sung 1 ). Trong khi hầu hết các trường hợp được ghi nhận xảy ra trước năm 2000 ( 66 ), các trường hợp nhập khẩu sốt Lass gần đây đã được báo cáo ở Hoa Kỳ [Pennsylvania ( 67 ), Minnesota ( 68 ) và Georgia ( 69 )], Ghana ( 70 ), Thụy Điển ( 71 ) và Đức ( 72 , 73). Một chủ đề phổ biến trong số các trường hợp này là, mặc dù chưa có nhiễm trùng thứ phát nào được ghi nhận, một giai đoạn thuyên giảm không liên tục giữa điều trị ban đầu và tái phát các triệu chứng có nguy cơ tiềm ẩn đối với bệnh kéo dài và lây truyền ( 74 ). Một thực tế nổi bật là arenavirus cũng có tiềm năng được sử dụng làm vũ khí sinh học ( 75 , 76 ) là mối quan tâm đặc biệt đối với các khu vực đặc hữu đang tham gia vào các cuộc xung đột chính trị và quân sự liên tục ( 77 ). Sự lây truyền từ người sang người, mặc dù rất hiếm khi xảy ra, đã được ghi nhận thông qua việc sử dụng các dụng cụ y tế bị ô nhiễm trong các thủ tục y tế tiêu chuẩn và chuyên khoa, chẳng hạn như ghép tạng ( 78). Nhìn chung, mối đe dọa lây lan và xuất khẩu arenavirus từ các khu vực lưu hành cần được quan tâm đối với các cân nhắc về sức khỏe cộng đồng bất chấp các rào cản tự nhiên hiện đang giúp ngăn chặn các vụ dịch lớn.
Vòng đời Arenavirus
Cơ chế xâm nhập của NW và OW Arenaviruses
Arenaviruses là các virus RNA chuỗi đơn bao bọc, ambisense. Cấu trúc của chúng bao gồm một màng bao chứa các tiểu đơn vị glycoprotein bề mặt (GP) bao quanh một capsid, bao gồm protein ma trận Z ( Hình 4A ). Bên trong capsid là RNA polymerase phụ thuộc L RNA (L RdRp) và bộ gen phân đoạn sinh học của virus được bao bọc bởi nucleoprotein (NP). Sự xâm nhập của tế bào được trung gian bởi GP, lần đầu tiên được biểu thị dưới dạng phức hợp tiền chất glycoprotein (GPC). Subilase chủ SK1-S1P phân giải protein GPC thành ba tiểu đơn vị cuối cùng của nó ( 79 - 81 ): GP1, GP2 và SSP (Peptide tín hiệu ổn định), tạo thành các dị thể trên bề mặt màng tế bào ( 82 - 84). GP1 hình thành các gai nhô ra khỏi vỏ virus và chịu trách nhiệm tương tác với các thụ thể đầu vào, trong khi GP2 là protein xuyên màng tổng hợp loại 1 nhờ vào miền 6 chuỗi xoắn của nó ( 85 , 86 ). SSP ( 87 ) là một protein tín hiệu nhỏ, kỵ nước và tồn tại lâu dài ( 88 ) có liên quan đến phản ứng tổng hợp virus ( 89 , 90 ), vận chuyển phức hợp GPC qua SK1-S1P chứa Golgi ( 91 ) và như một người đi kèm gấp GPC ( 92 , 93 ). Trong khi các arenavirus tái tổ hợp biểu hiện SSP từ một chủng khác là khả thi, thì các virut tái tổ hợp biểu hiện peptide tín hiệu không phải arenavirus lại không ( 94), cho thấy sự thích ứng cụ thể của SSP đối với protein arenavirus. Quan sát này được củng cố bằng công việc từ phòng thí nghiệm của chúng tôi, cho thấy dư lượng SSP nhất định làm tăng sự phát triển của virus độc lập với hiệu quả xâm nhập tế bào, minh họa nhiều vai trò của SSP trong vòng đời của virus vẫn chưa được làm rõ hoàn toàn ( 95 ). GP1 và GP2 cũng chứa dư lượng N-glycosyl hóa tại nhiều địa điểm ( 96 ), trong khi SSP là myristoylated ( 89 ). Mặc dù mục đích của các sửa đổi sau dịch mã này vẫn chưa được mô tả chi tiết, glycosyl hóa GP1 / 2 có liên quan đến vận chuyển protein của virus ( 96 ) và myristoylation SSP đã được tìm thấy là rất quan trọng để định hướng neo màng và phản ứng tổng hợp virus ( 89 , 90 ).
Hình 4. (A) Cấu trúc của các hạt arenavirus. (B) So sánh cơ chế xâm nhập của các arenavirus OW và NW. (C) Thời gian biểu hiện protein và sao chép RNA trong vòng đời của arenavirus được xác định bởi cấu trúc gen.
LASV và LCMV lần đầu tiên được phát hiện sử dụng α-dystroglycan làm thụ thể xâm nhập tế bào của họ ( 97 ), sau đó được xác nhận là trường hợp của tất cả các loại vi khuẩn OW và clade C NW arenavirus ( 98 ) ( Hình 4B ). Glycosyl hóa α-dystroglycan bằng glycosyltransferase LARGE là cần thiết để nhận biết bởi arenaviruses ( 99 - 101 ), bắt chước sự tương tác giữa α-dystroglycan và ligand laminin tự nhiên của nó ( 102 ). Sự điều hòa của α-dystroglycan dường như là một lực di truyền trong các vùng lưu hành của arenavirus, vì các nghiên cứu genom trên diện rộng đã tìm thấy bằng chứng về sự lựa chọn đa hình của LARGE và các protein điều hòa α-dystroglycan khác ở dân số Nigeria ( 103- 105 ). Tiểu đơn vị GP1 đầu C tương tác trực tiếp với α-dystroglycan ( 97 , 106 - 108 ), trong khi tiểu đơn vị GP2 đầu cuối C được phát hiện là rất quan trọng để ổn định phức hợp α-dystroglycan-GP ( 109 , 110 ). Dư lượng 260 trên GP1 là dư lượng đầu tiên được coi là quan trọng đối với tương tác với α-dystroglycan ( 98 , 111 - 113 ). Phân tích tinh thể học tia X sau đó đã xác định cấu trúc vòng 1 và đặc biệt là dư lượng 153, 155 và 190 của GP1, chịu trách nhiệm tương tác trực tiếp với α-dystroglycan ( 107). Dư lượng 260 và 136 cũng được coi là rất quan trọng đối với sự xâm nhập của tế bào, nhưng các dư lượng này đều nằm cách xa 25 Angstroms từ vòng 1. Do GP cần có chiều dài đầy đủ để xâm nhập tế bào, theo lý thuyết rằng các dư lượng bổ sung này có thể tạo điều kiện xâm nhập tế bào bằng các cơ chế phức tạp và chưa biết liên quan đến protein có chiều dài đầy đủ ( 107 ). Ủng hộ ý tưởng này, dư lượng tại giao diện trimeric của GP gần đây cũng được cho là rất quan trọng đối với mục nhập ô ( 108 ), nêu bật tầm quan trọng của GP đầy đủ đối với việc nhập ô hiệu quả.
Protein tế bào nội tiết LAMP1 đã được xác định là yếu tố chủ yếu quan trọng trong việc làm trung gian cơ chế chuyển đổi pH pH của màng tế bào vi rút và endocytosis của hạt virion, một phần có thể giải thích một số quan sát trước đây rằng các dòng tế bào gà là một trong số ít có thể bị nhiễm LASV vì chúng thiếu biểu hiện LAMP1 ( 106 , 114 ). Dư lượng histidine được bảo tồn trên tiểu đơn vị GP1 trong số các arenavirus của OW đã được tìm thấy để làm trung gian nhận biết bởi LAMP1 ( 108 ), và phân tích cấu trúc đã tìm thấy sự thay đổi trong cấu trúc GP1 sau khi tương tác với LAMP1, có thể đóng vai trò là cơ chế che giấu miễn dịch ( 115). Một cơ chế thú vị khác cũng đã được đề xuất đối với endocytosis LASV qua trung gian LAMP1, trong đó LAMP1 tăng ngưỡng pH cho endocytosis có tính axit, do đó làm tăng năng suất virus bằng cách ngăn chặn virus bằng môi trường axit bên trong endosome ( 116 ). Các yếu tố chủ khác và các thụ thể thay thế có thể thay thế cũng đã được xác định để xâm nhập các arenavirus có thể liên quan đến các chất trao đổi hydro natri ( 117 ) và các thụ thể phosphatidylserine Axl ( 118 ) và TIM-1 ( 119 ), cần phân tích thêm ( 120)). Một nghiên cứu gần đây cũng đã phát hiện ra rằng yếu tố NRP2 và CD63 của tế bào dường như đóng vai trò thay thế cho α-dystroglycan và LAMP1 để điều hòa sự xâm nhập của virus Lujo (LUJV) ( 121 ), liên quan đến việc bảo tồn các cơ chế tương tự trong các virus khác. tầm quan trọng của việc bảo tồn các cơ chế này trong quá trình tiến hóa của virus.
Các arenavirus sử dụng các thụ thể xâm nhập tế bào khác nhau tùy thuộc vào dòng họ. Clade B NW arenavirus gây bệnh ở người đã được tìm thấy sử dụng thụ thể transferrin của người 1 (hTrf1) ( 122 , 123 ) trong khi virus clade B không gây bệnh sử dụng orthologs hTrf1 ( 124 , 125 ). Một số thụ thể virus và các yếu tố chủ khác cũng đã được tìm thấy để cho phép virus Junin (JUNV) xâm nhập, với hTrf1 là thụ thể tế bào ứng cử viên chính ( 123 ) và DC-SIGN / L-SIGN ( 126 ), canxi điện áp các kênh ( 127 ) và các protein liên quan đến các con đường qua trung gian clathrin như con đường nội tiết dyn2 / Eps15 ( 128) là các yếu tố có thể. TRIM2 gần đây đã được xác định trong một màn hình siRNA là một chất ức chế sự xâm nhập của tế bào arenavirus theo cơ chế chưa được xác định ( 129 ). Các thụ thể cho các dòng khác của NA arenavirus vẫn chưa được biết, mặc dù đã chứng minh rằng các virus D clade dự kiến không sử dụng hTrf1 ( 130 ).
Các hạt virut xâm nhập vào tế bào bằng các con đường qua trung gian clathrin đối với các arenaviruses độc lập với α-dystroglycan ( 131 ) và một cơ chế độc lập với clathrin liên quan đến sự hình thành các thể đa bào qua trung gian PI3K trong quá trình endocytosis và con đường phân loại ESCRT virus ( 132 ) ( Hình 4B ). GP1 tách ra khỏi các hạt virus khi tiếp xúc với pH axit, làm lộ ra dư lượng GP2 trước khi hợp nhất virus ( 133 , 134 ). Sự hợp nhất virus sau đó xảy ra, trong đó các vùng kỵ nước trong GP2 ( 109 , 135 ) cũng như đuôi tế bào học ( 110 ) đã được tìm thấy có vai trò quan trọng.
Tái tạo bộ gen của virut, biểu hiện gen và hội
Sự sao chép bộ gen virut xảy ra trong cytosol sau khi nó được giải phóng khỏi endosome. Các protein NP và L của virus là các thành phần tối thiểu được biết đến cần thiết cho sự sao chép và sao chép bộ gen của virus ( 136 - 138 ), và protein Z của virus là một chất ức chế chức năng bắt đầu phiên mã của virus polymerase ( 137 - 140 ).
Các yếu tố cấu trúc RNA bộ gen của virus đóng vai trò quan trọng trong các cơ chế điều hòa của sự sao chép bộ gen của virus, sự phiên mã và biểu hiện gen. Vùng 5 ′ và 3 ′ chưa được dịch mã (UTR) của bộ gen arenavirus chứa các trình tự bổ sung được dự đoán để hình thành cấu trúc panhandle và được yêu cầu để sao chép và sao chép RNA virus hiệu quả ( 141 , 142 ). Cụ thể, 19 nucleotide nằm ở đầu 3 ′ UTR của bộ gen LCMV đã được tìm thấy để phục vụ như là một yếu tố khởi động được yêu cầu tối thiểu và các trình tự nằm ở 5 ′ UTR bổ sung để tạo thành cấu trúc panhandle dường như được yêu cầu để tổng hợp bộ gen hiệu quả ( 142). Foscaldi và các đồng nghiệp đã báo cáo rằng 5 ′ UTR của virus Tacaribe (TCRV) dường như có chứa tín hiệu kích thích tịnh tiến, trong khi một số trình tự trong 3 ′ UTR có thể điều chỉnh giảm biểu hiện gen virut ( 142 , 143 ). Các vùng biến đổi gen (IGR) xếp thành các cấu trúc thứ cấp của kẹp tóc được cho là giúp chấm dứt phiên mã ( 12 , 144 , 145 ) và để bảo vệ các bản sao mRNA của virus không polyadenylated khỏi sự thoái hóa của exoribonuclease tế bào ( 145 ). Các trình tự này dường như có dung sai lớn đối với các biến thể trình tự có thể được khai thác để phát triển các ứng cử viên vắc-xin suy yếu ( 21 , 146, 147 ). Đáng chú ý là trong quá trình sao chép bộ gen của virut, các đoạn genom trượt ngược từ vị trí gắn kết ban đầu của chúng, dẫn đến dư lượng 5 ′ ppGpp không được tạo khuôn ( 148 ) được cho là hoạt động như một mồi nhử RNA của virus bằng cách ức chế cạnh tranh RNA cảm giác bộ máy miễn dịch bẩm sinh tế bào ( 149 ). Các cơ chế phân tử của cảm giác RNA virus và các chiến lược trốn tránh miễn dịch bẩm sinh của arenavirus cũng như các nỗ lực phát triển vắc-xin sẽ được thảo luận chi tiết dưới đây.
Việc xác định vị trí của RNA arenavirus cũng được coi là quan trọng đối với việc kiểm soát sao chép, với cả RNA cảm giác và chống giác quan liên quan đến khoang tế bào chứa NP virus và các yếu tố chủ liên quan đến chuyển hóa RNA ( 150 ). Về vấn đề này, những tiến bộ gần đây trong hình ảnh DSRNA qua trung gian kháng thể ( 151 ) cũng như thăm dò cụ thể đối với RNA arenavirus genomic và chống genomic ( 152) cho thấy nhiều hứa hẹn để làm sáng tỏ tính năng động của RNA arenavirus trong vòng đời truyền nhiễm. Bằng chứng sơ bộ cho thấy rằng thời gian sao chép RNA của virus là theo cơ chế kiểm soát, vì các gen NP và L được phiên mã và dịch mã đầu tiên và trực tiếp từ bộ gen của virus cảm giác âm tính, trong khi GPC và Z được biểu hiện vài giờ sau khi RNA gen của virus các đoạn mã hóa các gen này đã được sao chép và sau đó được phiên mã ( 152 , 153 ) ( Hình 4 ). Ngoài ra, các tế bào bị nhiễm virus xuất hiện để khuếch đại các gen virut trong các đợt biểu hiện và thanh thải virus theo chu kỳ, cơ chế phân tử không rõ ràng ( 152). Các nghiên cứu trong tương lai trong lĩnh vực này sẽ bao gồm phát triển phương pháp và tối ưu hóa để hình ảnh các loài RNA ở số lượng bản sao thấp hơn và để mở rộng các tiết mục RNA có sẵn cho hình ảnh được nhắm mục tiêu.
Sau khi các RNA virus được sao chép, phiên mã và dịch mã, quá trình tổng hợp virion xảy ra và được trung gian bởi cả protein của virus và tế bào chủ. Các miền C-terminal của protein ma trận Z của virus là một người chơi trung tâm để lắp ráp virus, nảy chồi và giải phóng khỏi các tế bào bị nhiễm bệnh. Tương tác ZL ( 140 , 154 ), tương tác Z-NP ( 155 ) và tương tác Z-GP ( 156 , 157 ) đã được chứng minh để đảm bảo đồng địa hóa các protein virut để lắp ráp. Sau đó, Z tương tác với các protein con đường TsRT-101 ESCRT của tế bào để cho phép quá trình nảy chồi của virus bắt đầu ( 158 , 159), được hỗ trợ bởi dư lượng myristoylation tại đầu N của Z để cho phép tương tác với màng tế bào ( 160 , 161 ). Các protein Z cũng đã được tìm thấy có khả năng tự nảy chồi và tạo ra các virut giống như các hạt (VLP) khi không có RNA virus hoặc các protein khác cho thấy Z là cần thiết và đủ để nảy chồi ( 162 - 165 ). Một báo cáo gần đây cho thấy rằng các miền muộn nằm trong phần đầu C của protein Z cũng có thể được yêu cầu để giải phóng các hạt virion được gọi là khiếm khuyết (DI) từ các tế bào bị nhiễm bệnh nhưng không nhất thiết phải giải phóng sự lây nhiễm virion, một quá trình có thể được điều chỉnh bởi sự phosphoryl hóa một số dư lượng nhất định trong protein Z của virus (163 ). Các hạt DI được tạo ra bởi nhiều loại virut, bao gồm cả arenavirus, trong quá trình lây nhiễm và tương tự như các hạt virion truyền nhiễm về ngoại hình và hàm lượng protein nhưng chúng không thể tạo ra nhiễm trùng sản xuất ( 166 ) vì bộ gen của chúng có thể xóa lớn và khó hiểu ( 167 ). Việc xóa như vậy đã được quan sát ở các vùng 3'UTR của bộ gen LCMV và có khả năng ở nơi khác trong bộ gen của virus, nhưng chức năng cụ thể của chúng trong việc ức chế sự nhân lên của virus vẫn chưa được nghiên cứu chi tiết ( 168 ). Arenavirus đã được tìm thấy để tạo ra các hạt DI ở mức độ cao trong nuôi cấy tế bào ( 169 ) và trong các mô hình lây nhiễm động vật ( 170) và các hạt DI đã được lý thuyết hóa để góp phần vào sự tồn tại của virus ( 166 , 171 , 172 ).
Sinh bệnh học và ức chế miễn dịch của vật chủ
Hồ sơ bệnh Mammarenavirus có xu hướng không đồng nhất ( 173 - 176 ). Sốt Lass, bệnh arenavirus nặng nhất, ước tính gây ra tới 300.000 trường hợp và 5.000 ca tử vong mỗi năm ở các khu vực lưu hành ở Tây Phi ( 5 , 173 ). Một vụ dịch gần đây đã xảy ra ở Nigeria đã dẫn đến 431 trường hợp được xác nhận trong phòng thí nghiệm bao gồm 37 nhân viên y tế và với tỷ lệ tử vong chung là 25% ( 177 - 179 ). Các vụ dịch trước đó đã ghi nhận tỷ lệ tử vong thấp hơn ở bệnh nhân nhập viện ( 180 ). Tuy nhiên, tỷ lệ tử vong có thể lên tới 87% ở những phụ nữ bị nhiễm bệnh trong ba tháng thứ ba của thai kỳ ( 181), và việc truyền arenavirus từ mẹ sang thai đã được chứng minh trên các mô hình gặm nhấm ( 64 ) cũng như trong một trường hợp được báo cáo gần đây ở người ( 182 ). Nhiều biến chứng khác phát sinh từ nhiễm trùng arenavirus nghiêm trọng bao gồm tổn thương gan ( 183 - 186 ) và mạch máu ( 185 , 187 , 188 ), cả hai đã được tái tổ hợp trong mô hình động vật arenavirus lợn guinea ( 189 - 191 ) cũng như ở chuột bị suy giảm miễn dịch ( 192 , 193 ) và một mô hình chuột hamster mới lạ arenavirus ( 194). Trong khi tổn thương gan có xu hướng rất nổi bật trong nhiễm trùng do OW arenavirus với các yếu tố tiểu cầu và các sản phẩm phân hủy heme là dấu ấn sinh học quan trọng của bệnh LASV, xuất huyết và tổn thương mạch máu xảy ra thường xuyên hơn trong nhiễm trùng arenavirus ( 195 ) ( Hình 5 ). Mất thính giác giác quan (SNHL) cũng xảy ra ở 29% số người sống sót sau sốt Lassa ( 196 - 199 ) có thể được cho là do phản ứng viêm gây bệnh trong hệ thống thần kinh thính giác ( 200 , 201 ). Các biến chứng thần kinh khác cũng đã được báo cáo cho nhiễm trùng arenavirus ( 202 , 203 ).
Các tế bào đơn bào như đại thực bào phế nang và tế bào đuôi gai là mục tiêu sớm nhất để xâm nhập tế bào arenavirus. Tuy nhiên, các tế bào này không được kích hoạt khi có sự xâm nhập của virus, bằng chứng là sự thiếu tăng mức độ kích hoạt, như CD80, CD86, CD40, CD54 và HLAs cũng như cytokine TNFα, IL1β, IL6 và IL12 ( 204 , 205 ). Vì lý do này, các tế bào monocytic được cho là hoạt động như một ổ chứa virut, khi bị nhiễm virus, nơi virus có thể dễ dàng xâm nhập và virus sau đó lây lan khi các tế bào này xâm nhập vào các hạch bạch huyết ( 206 , 207 ). Sự thất bại của các tế bào này để được kích hoạt là phù hợp với quan sát của suy giảm miễn dịch tổng quát ở những người bị nhiễm nặng và gây tử vong ( 208, 209 ). Sự nhân lên của virus cũng đã được quan sát trực tiếp ở một số loại tế bào, bao gồm các tế bào biểu mô đường hô hấp sau khi nhiễm bệnh ở người ( 210 ) và mô hình động vật ( 211 ).
Các nghiên cứu về người sống sót và người gặm nhấm nhiễm mammarenavirus đều chỉ ra rằng hoạt động đúng của các phản ứng miễn dịch (miễn dịch qua trung gian tế bào T và tế bào T) là rất quan trọng để giảm thiểu tốc độ tăng trưởng của virus, biểu hiện triệu chứng và tỷ lệ tử vong ( 209 , 212 ). Phản ứng miễn dịch bẩm sinh là sự tổng hợp các cơ chế phòng vệ không đặc hiệu chống lại các kháng nguyên nước ngoài rất quan trọng để phát hiện sớm và ức chế sự phát triển của mầm bệnh trước khi đáp ứng miễn dịch thích nghi có thời gian để tạo ra miễn dịch qua trung gian tế bào thích hợp, như sự phát triển của kháng thể và gây độc tế bào Phản ứng tế bào lympho T (CTL) chống lại mầm bệnh xâm nhập và / hoặc các tế bào bị nhiễm mầm bệnh ( 212). Miễn dịch bẩm sinh được ban hành trong vòng vài giờ sau khi nhận ra vật chủ của mẫu phân tử liên quan đến mầm bệnh (PAMP). Các PAMPs virus phổ biến nhất được các tế bào miễn dịch nhận ra là các đặc điểm phân tử duy nhất của bộ gen virus, chẳng hạn như RNA 5 triphosphorylated và RNA sợi kép ( Hình 6 ). Các protein thụ thể nhận dạng mẫu (PRR), chẳng hạn như các thụ thể giống RIG-I (RLR) RIG-I và MDA5, được kích hoạt bởi PAMPs và dẫn đến biểu hiện cytokine và kích hoạt và tuyển dụng các tế bào miễn dịch bẩm sinh như đại thực bào, bạch cầu trung tính, và các tế bào đuôi gai ( 213 , 214 ).
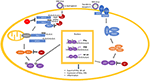
Hình 6. Các protein Arenavirus (NP và Z) ức chế các con đường RIG-I / MDA5 và NF-B. RIG-I và MDA5 được kích hoạt bởi PAMP DSRNA trong quá trình sao chép virus và được PACT tạo ra. Sau khi kích hoạt MAVS (trên ty thể) bởi RIG-I / MDA5, một dòng phân tử liên quan đến sự tương tác của IKKε và DDX3, sau đó là sự phosphoryl hóa các yếu tố phiên mã IRF3 và IRF7 để chuyển chúng vào nhân và liên kết với các vị trí liên kết yếu tố phiên mã của gen IFNα và IFNβ để kích hoạt phiên mã của chúng. Sự biểu hiện và xuất khẩu các sản phẩm gen này vào môi trường tế bào kích hoạt dòng tín hiệu IFN1 theo kiểu tự động hoặc paracrine để tạo ra biểu hiện của hàng trăm gen kích thích interferon (ISGs) và gen gây viêm để kháng virut. Con đường NF-κB được kích hoạt bằng cách nhận biết một số tính năng nhất định của các hạt virus bằng các thụ thể màng TLR 2 hoặc TLR 6. Điều này khởi tạo một tầng phân tử dẫn đến sự dịch chuyển của hai đơn vị NF-functionalB chức năng (p50 và p65) vào hạt nhân, dẫn đến sản xuất nhiều hơn nữa của NF-κB. Các protein Arenavirus (NP hoặc Z hiển thị màu đỏ) được biết là có tác dụng ức chế các bước khác nhau của các con đường RIG-I / MDA5 và NF-B bằng cách làm suy giảm các PAMP DSRNA (thông qua chức năng NP RNase) hoặc ức chế trực tiếp chức năng bình thường của các tế bào khác nhau protein (RIG-I, MDA5, PACT, IKKε hoặc p50 / p65). dẫn đến sản xuất nhiều hơn nữa của NF-κB. Các protein Arenavirus (NP hoặc Z hiển thị màu đỏ) được biết là có tác dụng ức chế các bước khác nhau của các con đường RIG-I / MDA5 và NF-B bằng cách làm suy giảm các PAMP DSRNA (thông qua chức năng NP RNase) hoặc ức chế trực tiếp chức năng bình thường của các tế bào khác nhau protein (RIG-I, MDA5, PACT, IKKε hoặc p50 / p65). dẫn đến sản xuất nhiều hơn nữa của NF-κB. Các protein Arenavirus (NP hoặc Z hiển thị màu đỏ) được biết là có tác dụng ức chế các bước khác nhau của các con đường RIG-I / MDA5 và NF-B bằng cách làm suy giảm các PAMP DSRNA (thông qua chức năng NP RNase) hoặc ức chế trực tiếp chức năng bình thường của các tế bào khác nhau protein (RIG-I, MDA5, PACT, IKKε hoặc p50 / p65).
RIG-I và MDA5, khi liên kết với PAMP DSRNA trong cytosol trong quá trình sao chép virus, thay đổi sự tuân thủ của chúng từ trạng thái đóng sang trạng thái mở và kích hoạt ( 215 ). Các RLR được kích hoạt (RIG-I và MDA5) khởi tạo một số dòng phân tử phức tạp, bao gồm kích hoạt protein tín hiệu chống virut ty lạp thể (MAVS), cuối cùng dẫn đến sự dịch chuyển các yếu tố phiên mã như các yếu tố điều hòa interferon (IRF) IRF3 và IRF3 cũng như yếu tố hạt nhân kappa B (NF-kB) vào nhân của các tế bào để kích hoạt sự biểu hiện của interferon loại 1 (IFN1) bao gồm IFNα và IFNβ, và nhiều loại gen kích thích interferon (ISG) ( 216 , 217). Một nghiên cứu gần đây đã gợi ý rằng IFNα có thể chủ yếu liên quan đến việc ức chế sự phát triển của virut trong giai đoạn đầu của nhiễm virut, trong khi IFNβ có thể kiểm soát sự phát triển của virut trong giai đoạn nhiễm trùng sau này ( 218 ). IFN1 sau đó được tiết ra và ràng buộc bởi các thụ thể của chúng (IFNAR) trên bề mặt của cùng một tế bào hoặc các tế bào lân cận, kích hoạt tầng tín hiệu IFN trong một vòng phản hồi tích cực để tạo ra nhiều IFN1 và các sản phẩm gen chống vi rút để truyền kháng vi rút ( 219 , 220 ).
Nhiễm trùng arenavirus (ví dụ, LASV) ở những bệnh nhân có triệu chứng từ trung bình đến nặng có liên quan đến sự ức chế đáp ứng miễn dịch bẩm sinh với mức độ giảm IFN1 và các cytokine gây viêm ( 184 , 221 , 222 ) ( Hình 5 ). Tầm quan trọng của việc truyền tín hiệu IFN1 để kiểm soát arenavirus dường như được bảo tồn ở động vật có vú, vì chuột dại (WT) không biểu hiện triệu chứng trong khi nhiễm arenavirus nhưng chuột bị loại bỏ thụ thể IFNAR (IFNAR) đã bị phát hiện mắc bệnh ( 223 ) 224 ). Ngoài ra, nhiễm trùng in vivo đối với các loài linh trưởng không phải người (NPH) và chuột lang với LASV Soromba chủng phân lập từ các loài gặm nhấm địa phương ở Mali, Châu Phi, cho thấy sự gia tăng đáng kể tín hiệu cytokine và giảm tỷ lệ tử vong so với các chủng LASV khác ( 8 ). Những con chuột bị nhiễm OW LCMV, có khả năng duy trì sự lây nhiễm dai dẳng với mức tín hiệu IFN1 thấp ( 225 , 226 ), hiển thị một đợt bùng phát IFN1 sau 6 giờ 48 giờ sau khi bị nhiễm bệnh và 2 phút4 trước khi đạt cực đại về chuẩn độ virus, cho thấy rằng Tín hiệu IFN1 là quan trọng nhất để ức chế sự tăng sinh của virus trong giai đoạn sớm nhất của nhiễm trùng ( 209 , 227). Sự khác biệt giữa các phản ứng miễn dịch ở loài gặm nhấm và con người là một trong những khía cạnh quan trọng của các cuộc điều tra tích cực. Các bể chứa động vật gặm nhấm thường không gặp phải các triệu chứng nghiêm trọng do nhiễm trùng arenavirus OW ( 65 , 228 , 229 ) và chuột phải được điều trị miễn dịch để trải nghiệm các triệu chứng quan trọng. Chuột bị nhiễm LASV cũng trải qua quá trình điều hòa sớm các phân tử bám dính tế bào trong các tế bào đơn nhân máu ngoại vi (PBMC) phù hợp với các tế bào miễn dịch được tuyển dụng vào vị trí nhiễm trùng ( 230 ). Các arenavirus của NA khác với các chủng OW ở chỗ chúng có xu hướng tạo ra mức độ IFN1 và cytokine tăng lên, và một phản ứng chống viêm được ưa chuộng để ức chế sự tăng sinh của virus ( 222 , 231- 234 ) ( Hình 5 ). Nuôi cấy tế bào A549 bị nhiễm virus ( 235 , 236 ) cũng như bệnh nhân nhiễm trùng gây tử vong ( 237 - 239 ) đã được chứng minh là có mức độ IFN1 và TNFα được điều chỉnh tăng liên tục. Tuy nhiên, các đại thực bào bị nhiễm in vitro với các arenavirus không thể hiển thị sự điều hòa này ( 240 ).
Các NP arenavirus đã được tìm thấy để ức chế con đường RIG-I / MDA5. Cấu trúc tinh thể của NP LASV và các nghiên cứu chức năng tiếp theo đã tiết lộ miền 3′-5 ′ exoribonuclease nằm trong miền đầu C của nó ( 241 - 243 ), làm giảm đáng kể DSRNA ( 242 , 244 ). Đầu cuối N của NP chứa một miền duy nhất liên kết ssRNA ( 245 ) và đã được đề xuất để liên kết với cấu trúc nắp mRNA m7GpppN ( 241 ). NP tương tác trực tiếp với RIG-I và MDA5 ( 246) và công trình gần đây từ phòng thí nghiệm của chúng tôi đã chứng minh rằng NP ngăn chặn sự tăng cường chức năng RIG-I bằng protein PACT của tế bào và miền exoribonuclease của NP là cần thiết cho sự ức chế này ( 247 ), cơ chế phân tử sẽ được thảo luận chi tiết trong phần tiếp theo Miền exoribonuclease cũng được yêu cầu để ức chế NP của protein kinase IKKε ( 248 ) và các protein tế bào khác trong con đường IRF ( 249 , 250 ). Việc hủy bỏ miền exoribonuclease đã cho phép biểu hiện IFN1 ở các đại thực bào và tế bào đuôi gai bất hoạt ( 251 , 252 ) và kích hoạt các tế bào giết người tự nhiên (NK) sau đó dẫn đến hiện diện kháng nguyên (253 ). Ngoại lệ cho NP-mediated IFN1 ức chế dường như là Tacaribe virus (TCRV) NP ( 254 ), mà ban đầu được cho là do khác biệt trong 4 dư lượng exoribonuclease tìm thấy trong protein của virus này ( 255 ). Tuy nhiên, cả hai nghiên cứu về cấu trúc và chức năng sau đó đã chứng minh rằng NP TCRV có thể làm suy giảm hiệu quả DSRNA và ức chế con đường IFN1 ( 244 , 255 ). Những nghiên cứu này chỉ ra tầm quan trọng của sự suy giảm PAMP DSRNA của các NP arenavirus đối với sự ức chế con đường IFN1.
Một xem xét quan trọng trong việc xác định vai trò lớn hơn của NP trong sinh bệnh học arenavirus là thực tế là sự ức chế IFN1 của NP cũng có trong các chủng không được biết là gây bệnh cho người. Ví dụ, NP từ virus Pichinde không gây bệnh (PICV) đã được tìm thấy để ức chế con đường IFN1 trong tế bào người ( 254 ). Ngoài ra, công việc từ phòng thí nghiệm của chúng tôi đã chứng minh rằng mỗi trong số 5 dư lượng xúc tác exoribonuclease (RNase) là cần thiết để ức chế IFN1 bởi NP Pichinde cũng như cho sự tăng trưởng PICV tối ưu trong ống nghiệm ( 256 ). Các virus đột biến miền RNase cũng đã được tìm thấy cho thấy tải lượng virus giảm và sinh bệnh học trong cơ thể ở chuột lang (thường gây tử vong cao, phát triển các triệu chứng giống như sốt xuất huyết ở người và hỗ trợ tải lượng virus cao khi bị nhiễm bởi chủng P18 PICV), và thậm chí dẫn đến việc tạo ra virut hồi phục WT ( 256), ngụ ý vai trò quan trọng của chức năng NP RNase để sao chép virus tối ưu. Nhìn chung, khả năng NP ức chế biểu hiện IFN1 bằng cách làm giảm PAMP DSRNA có khả năng được bảo tồn trên các arenavirus đã biết. Bằng chứng là sự kiểm soát chặt chẽ biểu hiện gen và định vị RNA virus trong các tế bào, rõ ràng việc điều chỉnh nồng độ RNA và nội địa hóa là một cơ chế quan trọng của vòng đời virus để cho phép sao chép tối đa mà không bị dập tắt sớm trong chu kỳ đáp ứng miễn dịch bẩm sinh, có thể giải thích sự bảo tồn tuyệt đối ức chế IFN1 bằng protein NP arenavirus.
Các nghiên cứu gần đây cũng đã tập trung vào vai trò của protein Z của virus trong việc ức chế con đường IFN1. Ban đầu, các protein Z từ 4 chủng arenavirus đã được thử nghiệm [JUNV, virus Machupo (MACV), TCRV và virus Sabia (SABV)] nhưng không phải từ các chủng OW LASV hoặc LCMV đã được tìm thấy để tương tác trực tiếp với RIG-I và ức chế IFN1 biểu thức ( 257 ). Gần đây, phòng thí nghiệm của chúng tôi đã chứng minh rằng protein Z từ cả hai chủng arenavirus OW và NW được biết là gây bệnh ở người có thể tương tác trực tiếp với RIG-I để ức chế biểu hiện IFN1, nhưng protein Z từ virus arenavirus không gây bệnh không thể ( 258). Những kết quả này đã được tóm tắt lại trong các đại thực bào nguyên phát ở người bị nhiễm WT và PICV chimeric cho thấy rằng N-terminator của LCMV Z là đủ để ức chế kích hoạt đại thực bào khi được biểu thị dưới dạng protein Z của chimeric với PICV không gây bệnh ( 259 ). Nhìn chung, protein Z đang nổi lên như một mục tiêu quan trọng khác trong việc nghiên cứu cơ chế ức chế miễn dịch bẩm sinh của arenavirus, và một yếu tố tiềm năng đáng khích lệ trong sinh bệnh học (nghĩa là yếu tố độc lực tiềm tàng) sẽ cần đặc tính hơn nữa ( 105 , 260 ) .
Một lĩnh vực nghiên cứu với sự chú ý ngày càng tăng là vai trò của các tế bào miễn dịch bẩm sinh và các cytokine trong việc bắt đầu phản ứng miễn dịch thích nghi chống lại nhiễm trùng mammarenavirus. Một mô hình quan trọng xuất hiện từ các nghiên cứu sơ bộ là khả năng ức chế đáp ứng miễn dịch bẩm sinh của arenavirus có vẻ tương quan tích cực với khả năng ngăn chặn bất kỳ phản ứng miễn dịch thích nghi nào sau đó. Mối tương quan giữa đáp ứng miễn dịch bẩm sinh bị ức chế với đáp ứng tế bào T bị suy giảm và chậm trễ trong những trường hợp mắc bệnh này với nhiễm arenavirus gây tử vong đã được chứng minh ở người ( 210 , 261 , 262 ), linh trưởng không phải người ( 221 ), lợn guinea ( 47 , 190 , 211 , 263 - 265 ), chuột suy giảm miễn dịch ( 223 , 224 , 266 ) cũng như ở chuột suy giảm miễn dịch được cấy ghép tế bào từ tủy xương chuột WT ( 193 ). Theo đó, các cá nhân sống sót sau khi nhiễm arenavirus có thể giữ được tải lượng virus ở mức thấp, đạt đỉnh 1020 ngày sau khi bị nhiễm LASV, trong khi các cá nhân không chịu được tải lượng virus liên tục tăng theo cấp số nhân ( 205 , 221 , 261 , 262 , 267 - 269). Ở chuột WT, LCMV tạo ra sự biểu hiện mạnh mẽ của các cytokine chính như IFN loại I và II cũng như IL-18, việc sản xuất IFN loại II phụ thuộc vào tế bào T CD8 ( 270 ). Điều này không chỉ minh họa sự kết nối chặt chẽ giữa các phản ứng miễn dịch bẩm sinh và thích nghi, mà còn minh họa thêm về cách đáp ứng miễn dịch chủ động là chìa khóa cho sức đề kháng tự nhiên chống nhiễm trùng arenavirus ở chuột. Tầm quan trọng của giao diện thích ứng bẩm sinh cũng được mô tả lại trong mô hình đồng nhiễm gần đây của LCMV và E. Coli , chứng minh rằng cơ chế ức chế do LPS gây ra của các tế bào NK làm suy giảm đáng kể phản ứng tế bào CD8 T cụ thể của LCMV và sức sống của chuột bị nhiễm bệnh ( 271 ).
Các tế bào T CD8 đã được tìm thấy là không thể thiếu để loại bỏ các arenavirus ( 221 , 272 - 279 ), trong khi các phản ứng tế bào T CD4 ( 277 , 280 ) và kháng thể ( 184 ) đã được phát hiện. Trên thực tế, một yếu tố đóng góp tiềm năng đối với khả năng gây bệnh của arenavirus cũng như sự thất bại của hầu hết các ứng cử viên vắc-xin arenavirus trước đây trong việc bảo vệ chống lại các chủng gây bệnh có thể là phản ứng tế bào T CD4 +. Chuột STAT1 KO chỉ có thể sống sót khi bị nhiễm LCMV khi tế bào T CD4 + bị cạn kiệt ( 266), cho thấy rằng việc thiếu tín hiệu IFN bằng cách nào đó có thể cực kỳ ủng hộ sự tăng sinh tế bào T CD4 + gây chết người. Việc xác định cơ chế gây chết tế bào T CD4 +, cho dù đơn giản là do ít tế bào T CD8 được kích hoạt hoặc thông qua một số cơ chế mới của tế bào T CD4, vẫn chưa được xác định.
Các tế bào đuôi gai (mDC) là thành phần quan trọng trong giao diện đáp ứng miễn dịch thích nghi bẩm sinh do kết hợp với kích thước quần thể lớn ( 281 ), kích hoạt mạnh mẽ các tế bào T CD8 ( 282 ) và sản xuất IFN1 dưới dạng CD8 T chất tăng cường kích hoạt -cell trong các điều kiện nhất định, chẳng hạn như trong khi nhiễm LCMV ( 283 ). Các tế bào đuôi gai (DC) là mục tiêu chính của nhiễm trùng bởi LASV ( 204 , 205 ), nhưng giống như các đại thực bào, chúng không được kích hoạt bởi nhiễm trùng ( 204 , 205). Tuy nhiên, tính năng này không nhất quán giữa các chủng arenavirus, như đã được chứng minh bằng mô hình so sánh được chứng minh bằng văn bản về khả năng miễn dịch mammarenavirus của LASV và virus Mopeia (MOPV). Cả hai đều là OW arenavirus và chia sẻ 75% axit amin và chuột Mastomys natalensis ở châu Phi như một ổ chứa virus (23). Tuy nhiên, MOPV không gây bệnh ở người và đã được coi là một ứng cử viên vắc-xin LASV tiềm năng ở các loài linh trưởng không phải người ( 284 ) và không có trường hợp nhiễm MOPV nào ở người được ghi nhận ( 285 ). Các nghiên cứu ban đầu cho thấy nhiễm MOPV của các tế bào đuôi gai có nguồn gốc monocyte (MoDCs) gây ra kích hoạt vừa phải và tăng sinh tế bào T CD8 đáng kể trong hệ thống nuôi cấy tế bào MoDC / T ( 286 , 287), trong khi các MoDC bị nhiễm LASV gây ra kích hoạt thấp và phản ứng tế bào T yếu và chậm ( 204 , 287 ).
Gần đây, cùng một nhóm các nhà nghiên cứu đã chứng minh rằng cả LASV và MOPV đều không thể sao chép tốt trong các tế bào đuôi gai (mDC) được phân lập trực tiếp từ PBMC và do đó, tạo ra mức sản xuất IFN1 rất thấp và các tế bào bị nhiễm LASV có thể không kích hoạt các tế bào T trong hệ thống nuôi cấy tế bào mDC / T ( 288 ). Tuy nhiên, MOPV có thể tạo ra mức IFN1 cao hơn và các cytokine được tiết ra được biết là gây ra hoạt hóa tế bào T so với các tế bào bị nhiễm LASV trong hệ thống nuôi cấy, mặc dù có sự tham gia của các tế bào đơn nhân và các loại tế bào khác có trong nuôi cấy hệ thống như là kết quả của tạp chất không thể loại trừ hoàn toàn. Bất kể, quan sát dường như chứng thực những phát hiện trước đó cho thấy rằng DC có thể phân phối để kích hoạt tế bào T trong khi nhiễm LCMV (289 ). Giống như LASV, LCMV được biết là ức chế đáp ứng miễn dịch bẩm sinh như đã được chứng minh trong một nghiên cứu khác ( 290 ).
Sử dụng virus chimeric mang các gen khác nhau từ LASV hoặc MOPV trên di truyền ngược LASV (RG) hoặc xương sống MOPV RG, cùng một nhóm các nhà điều tra đã chỉ ra rằng LASV NP là yếu tố quyết định chính trong việc ngăn chặn sản xuất IFN1 bằng mDCs ( 288 ), trong đó phù hợp với khả năng đã biết của tất cả các NP arenavirus đã biết để làm suy giảm PAMP RNA thông qua miền RNase được mã hóa của chúng và do đó ngăn chặn sản xuất IFN1 ( 105 , 241 , 244 , 247 , 252 - 256 , 291). Do thực tế là các mDC dường như không hỗ trợ sao chép sản xuất LASV và MOPV, rất khó để xác định liệu tác dụng ức chế IFN1 có phải là do sự biểu hiện của protein virut trong các tế bào bị nhiễm bởi các virut tinh bột khác nhau hay không. Hơn nữa, dữ liệu không thể giải thích sự khác biệt của kiểu hình mDC trong hệ thống nuôi cấy tế bào mDC / T giữa các bệnh nhiễm virut tinh tinh LASV và MOPV. Trong nỗ lực đưa ra lời giải thích tiềm năng cho quan sát này, các tác giả đã đưa ra rằng các hiệu quả khác nhau của các miền NP RNase của các arenavirus khác nhau để ngăn chặn sản xuất IFN1 có thể giải thích sự khác biệt giữa các arenavirus để kích hoạt tế bào T qua trung gian DC. Tuy nhiên, giả thuyết này cần được thử nghiệm chính thức.
Một LASV tinh tinh với sự thay thế GP của nó bằng MOPV đã được tìm thấy làm tăng đáng kể việc sản xuất IFN1 ( 288 ), có thể phản ánh các cơ chế phát hiện virus khác nhau dựa trên các thụ thể miễn dịch bẩm sinh khác nhau ( 106 ). Một ví dụ, dị vòng TLR2 / TLR6 giống như Toll đã được tìm thấy có trách nhiệm kích hoạt miễn dịch bẩm sinh bằng cách nhận ra GP của NA JUNV khi bị nhiễm virut để tạo ra phản ứng miễn dịch bẩm sinh ( 292 ) và phản ứng miễn dịch ( 293 ) ( Hình 6 ), trong khi chỉ có TLR2 có liên quan đến hoạt động chống vi-rút của OW arenaviruses ( 294 , 295). JUNV và các arenavirus khác của NA cũng đã được tìm thấy để bắt đầu quá trình apoptosis phụ thuộc caspase ( 233 , 296 - 298 ), trong khi OW arenavirus không gây ra apoptosis ( 204 , 298 ) hoặc gây ra apoptosis bị trì hoãn đáng kể ( 299 ) ( Hình 5 ). Sự đóng góp tương đối của các con đường được trung gian trực tiếp bởi thụ thể tế bào cụ thể và các cơ chế báo hiệu virus khác cần được đặc trưng hơn nữa trong các nghiên cứu trong tương lai.
Trái ngược với những phát hiện trước đó ( 258 , 259 ), protein Z không được tìm thấy trong mô hình virus chimeric LASV / MOPV để thể hiện tác dụng đáng kể trong việc ức chế miễn dịch ( 288 ), có thể được quy cho các mô hình lây nhiễm khác nhau đang được sử dụng. Điều đáng chú ý là các thí nghiệm với virut chimeric không xem xét mức độ biểu hiện gen khác biệt tiềm năng của protein virut trong các tế bào bị nhiễm virut trong bối cảnh xương sống của virut chimeric. Ngoài ra, vì các mDC dường như không hỗ trợ sao chép virus sản xuất, nó đã đặt ra một câu hỏi liệu có bất kỳ protein virus nào được tổng hợp trong mô hình mDC bị nhiễm virus hay không ( 288). Do đó, rất khó để phân biệt rõ ràng vai trò của protein virut riêng lẻ trong việc điều chỉnh miễn dịch kháng vi-rút trong mô hình nhiễm virus in vitro độc đáo này ( 288 ).
Điều chế các chức năng protein bẩm sinh của Arenavirus và các loại virus khác
Một tương tác mammarenavirus-host khác có ảnh hưởng đến sản xuất IFN1 là với protein PACT của tế bào ( Hình 6 ). PACT là một protein 313-aa có chứa 3 mô-típ bảo tồn dsRNA ràng buộc (dsRBMs) với dsRBM1 và 2 gắn vào RNA mạch kép và dsRBM3 trung gian kích hoạt của PKR kinase RNA mạch kép phụ thuộc vào ( 300 ). PACT đã được chứng minh là kích hoạt RIG-I thông qua tương tác với miền ức chế đầu cuối C của RIG-I và kích hoạt chức năng ATPase của nó để tăng cường sản xuất IFN1 khi nhiễm virus ( 301 , 302 ). Mặc dù PACT ban đầu được xác định là đối tác liên kết tế bào và chất kích hoạt protein của PKR ( 303 ), việc kích hoạt RIG-I bởi PACT không yêu cầu PKR ( 302). Tương tự như vậy, trong khi PACT cũng được chứng minh là có khả năng tương tác và kích thích protein Dicer của tế bào ( 303 , 304 ), Dicer dường như không đóng vai trò quan trọng trong việc điều hòa phản ứng chống virut qua PACT ( 302 ).
Mặc dù PACT và RIG-I kết hợp với nhau trong các thử nghiệm đồng kích thích miễn dịch, nhưng không rõ liệu sự tương tác này xảy ra nghiêm ngặt thông qua tương tác protein-protein hoặc bởi cả hai protein liên kết với RNA của virus và / hoặc tế bào hoặc kết hợp cả hai. Vai trò tiềm năng của RNA trong việc kích hoạt các protein miễn dịch bẩm sinh của tế bào (RIG-I và PACT) đã được chứng minh mạnh mẽ trong các phát hiện gần đây rằng các NP arenavirus đòi hỏi một miền liên kết DSRNA còn nguyên vẹn cũng như hoạt động exoribonuclease 3′-5 của nó để ngăn chặn PACT tăng cường chức năng RIG-I ( 189 - 191 ) ( Hình 6 ). Một số nucleoprotein virus khác có thể ngăn chặn sự tăng cường PACT của chức năng RIG-I, cũng đòi hỏi một miền liên kết DSRNA còn nguyên vẹn ( 305 - 307), hoặc trong trường hợp virus herpes simplex 1 (HSV1), độc lập với khả năng liên kết RNA của nucleoprotein ( 308 ). Gần đây, phòng thí nghiệm của chúng tôi đã chỉ ra rằng các NP arenavirus ngăn chặn sự tạo thành RIG-I bằng PACT, và miền exoribonuclease là bắt buộc ( 247). Tuy nhiên, NP dường như không tác động tiêu cực đến tương tác trực tiếp PACT / RIG-I, cho thấy NP có thể ức chế gián tiếp PACT bằng cách làm giảm DSRNA có thể liên quan đến phức tạp và rất cần thiết cho chức năng phù hợp của nó. Khi kết hợp với nhau, có vẻ như hầu hết nếu không phải tất cả các đối tác protein virut đã biết của PACT (cũng như chính PACT và đối tác protein tế bào của nó RIG-I) đều có các đặc tính gắn RNA, nhưng vẫn chưa hoàn toàn rõ ràng liệu liên kết DSRNA có phải là một yêu cầu tuyệt đối để ức chế kích hoạt RIG-I do PACT gây ra. Các nghiên cứu này cho thấy sự thiếu hiểu biết chi tiết về vai trò của các protein virut khác nhau, bao gồm NP arenavirus, để ức chế hoạt hóa RIG-I qua trung gian PACT và bản chất của các DSRNA (virut, tế bào hoặc cả hai) tham gia vào quá trình này. Các nghiên cứu trong tương lai về vai trò chính xác và cơ chế phân tử của các tương tác giữa virus-chủ thông qua con đường PACT / RIG-I có thể đóng vai trò là mục tiêu trị liệu chống vi-rút hấp dẫn để phát triển. Ngoài ra, các thuốc chống siêu vi nhắm mục tiêu PACT có thể ảnh hưởng đến tín hiệu căng thẳng NF-κB và p53 qua trung gian PACT-PKR (300 , 309 - 316 ) không chỉ tác động đến việc kiểm soát vi-rút mà cả các quá trình tế bào đã biết khác liên quan đến ung thư và các tình trạng sinh lý và trao đổi chất khác.
Phát triển vắc-xin cho và thuốc chống siêu vi chống lại nhiễm trùng Arenavirus
Hiện tại, loại vắc-xin chống vi-rút thành công duy nhất trên lâm sàng là chủng Anti-JUNV Candid # 1, hiện đang được sản xuất bởi chính phủ Argentina nhưng không được xem xét sử dụng ở quy mô lớn do dân số mục tiêu hạn chế ( 222 ) chỉ có ở Argentina là đặc hữu cho nhiễm trùng JUNV. Để tạo ra Candid # 1, một dòng virus phân lập ở người ( 317 ) đã được sử dụng để truyền hai lần ở chuột lang, sau đó là các đoạn bổ sung trong việc nuôi chuột và nuôi cấy tế bào ( 318 - 323 ). Một số đột biến duy nhất ở Ứng cử viên số 1 ban đầu được cho là làm suy giảm Ứng viên số 1 so với chủng WT của cha mẹ ( 323 , 324) và một đột biến như vậy (F427I trong miền xuyên màng của tiểu đơn vị GP2) luôn được tìm thấy là đủ để suy giảm ( 325 , 326 ). Mặc dù cơ chế cho sự suy giảm này vẫn chưa được làm sáng tỏ, người ta cho rằng đột biến có thể ảnh hưởng đến phản ứng tổng hợp hoặc hiệu quả trưởng thành của virus ( 325 ). Đột biến tương đương (F438I) ở virus Machupo (MACV) cũng được tìm thấy bị suy giảm ở chuột ( 327 ), cho thấy cơ chế suy giảm này có thể được bảo tồn cao. Ngoài ra, sự hiện diện của đột biến trong tiểu đơn vị SSP cùng với đột biến F427I trong GP2 được cho là ngăn chặn virus quay trở lại trình tự kiểu hoang dã của nó ( 326). Thật hấp dẫn khi giả định rằng các kỹ thuật suy giảm tương tự có thể được áp dụng cho sự phát triển của các loại vắc-xin arenavirus khác. Tuy nhiên, chúng có thể bị giới hạn trong vắc-xin JUNV vì một số lý do. Trong khi con đường IFN1 (đặc biệt là IFNβ) và phản ứng tế bào T tiếp theo đã được tìm thấy là rất quan trọng trong việc kiểm soát nhiễm trùng arenavirus ở chuột ( 193 , 209 , 223 , 224 , 231 , 266 , 270 , 328 ), kết quả ức chế miễn dịch liên quan đến arenavirus trong các phản ứng tế bào T hạn chế ( 184 , 204 , 221 , 222 , 279 , 287 ). Hơn nữa, JUNV GP đã được tìm thấy có chứa ít glycans hơn GP từ các mammarenaviruses khác ( 320 , 329 ) và dư lượng glycan trên LASV GP giàu glycan đã được chứng minh là có tác dụng thúc đẩy trốn kháng thể trung hòa ( 330 ). Điều này được củng cố bởi các quan sát gần đây rằng các kháng thể chống JUNV từ các bệnh nhân bị nhiễm bệnh có thể vô hiệu hóa các chủng JUNV khác nhưng không thể cung cấp sự trung hòa chống lại các arenavirus khác ( 331 ).
Một phần do những lý do đã nói ở trên, việc phát triển các loại vắc-xin hiệu quả chống lại các mammarenavirus gây bệnh khác (ngoài JUNV) đã được chứng minh là khó khăn hơn nhiều. Một nỗ lực ban đầu là sử dụng các hạt LASV được chiếu xạ gamma, tạo ra các phản ứng hài hước đáng kể trong NHP nhưng không bảo vệ được trước thách thức LASV gây tử vong ( 332 ). Một chủ đề tương tự đã được ghi nhận trong các nghiên cứu tiếp theo, trong đó miễn dịch thích ứng [và thậm chí miễn dịch bảo vệ chéo ( 333 )] đã được tạo ra ở các đối tượng được tiêm chủng, nhưng đã thất bại trong việc bảo vệ chống lại thách thức virus gây chết người. Các chiến lược di truyền ngược lại đang được khám phá để vượt qua một số trở ngại này, chẳng hạn như tối ưu hóa codon để tăng biểu hiện kháng nguyên protein của virus ( 334), Vectơ arenaviral tri-phân đoạn trên LCMV ( 335 - 339 ) hoặc PICV ( 340 , 341 xương sống để tăng sự suy giảm của virus), và chu trình đơn vectơ arenaviral ( 342 , 343 ) để giảm thiểu suy giảm miễn dịch thông qua sao chép của virus mũ.
Một phương pháp khác để sản xuất vắc-xin ứng cử viên đang phát triển dựa trên một loại virut được phân loại lại là ML29, chứa phân đoạn gen L của MOPV và phân đoạn gen S của LASV ( 269 , 291 , 344 - 346 , 418 - 420 ) ( Hình 3 ) . Người ta đã xác định rằng các biểu hiện kháng nguyên của LASV NP và GP từ virut tái tổ hợp này là rất cần thiết để cung cấp khả năng miễn dịch bảo vệ mạnh mẽ cho các loài gặm nhấm (ví dụ, chuột lang) và NHPs (ví dụ, marmosets và Rhesus maca) chống lại bệnh chết người do nhiễm LASV ( 344 - 347). Các hạt DI được tạo ra bởi các tế bào bị nhiễm liên tục với ML29 cũng đã được tìm thấy gây cản trở sự sao chép của LASV, MOPV và LCMV, và tạo ra khả năng miễn dịch qua trung gian tế bào mạnh ở chuột STAT1 KO ( 348 ), cho thấy tiềm năng hình thành ML29 với nó DI hướng tới sự phát triển của vắc-xin pan-arenavirus. Các loại vắc-xin ứng cử viên LASV khác bao gồm những loại biểu hiện kháng nguyên LASV GP hoặc NP từ bộ gen của các loại virut tái tổ hợp khác nhau, chẳng hạn như Virus viêm miệng Vesicular (VSV) ( 349 , 350 ), virus vaccinia ( 351 , 352 ), MOPV ( 291 ), Virus sốt vàng 17D ( 353 , 354 ), bản sao alphavirus ( 355 , 356 ) và virus dại bất hoạt ( 357 ), tất cả chúng đã được chứng minh là có hiệu quả bảo vệ khác nhau chống lại nhiễm trùng LASV trong các mô hình động vật khác nhau. Các nỗ lực phát triển vắc-xin LASV khác, được hỗ trợ bởi một tổ chức quốc tế phi lợi nhuận có tên là Liên minh đổi mới phòng chống dịch bệnh (CEPI), bao gồm những hoạt động dựa trên nền tảng vắc-xin mới, chẳng hạn như vắc-xin dựa trên vi-rút sởi tái tổ hợp ( 358 ) và vắc-xin dựa trên DNA ( 359 , 360). CEPI cũng đã hỗ trợ hai ứng cử viên vắc-xin LASV khác dựa trên các vec tơ dựa trên rVSV tái tổ hợp. Đầu tiên là cấu trúc rVSV thể hiện kháng nguyên LASV GP dựa trên cùng một nền tảng được áp dụng để thể hiện EBOV GP như một kháng nguyên vắc-xin được sử dụng trong thử nghiệm tiêm chủng vòng ở Guinea, Châu Phi ( 361 , 362 ). Thứ hai là một cấu trúc rVSV-LASV GP khác với gen VSV-N được phiên mã và đuôi tế bào chất VSV-G bị cắt ngắn được thiết kế để tăng độ an toàn của vắc-xin. Các vec tơ rVSV suy yếu tương tự biểu hiện một hoặc nhiều GP EBOV đã được chứng minh là có khả năng miễn dịch trong NHP ( 363 ) và bảo vệ thành công NHP trước thách thức virus EBOV và Marburg ( 364 - 366), nhưng hiện tại không có dữ liệu tiền lâm sàng được công bố để hỗ trợ phát triển vắc-xin Lassa dựa trên nền tảng này. CEPI gần đây cũng đã trao một hợp đồng phát triển tiền lâm sàng cho một cấu trúc LASV-GP khác trên xương sống của một simen adenovirus không sao chép, nhưng một lần nữa không có thông tin tiền lâm sàng nào về sự phù hợp của nền tảng virus này đối với sự phát triển vắc-xin Lass ( 367). Vẫn còn phải xem các vắc-xin được hỗ trợ bởi CEPI sẽ hoạt động tốt như thế nào trong những năm tới. Một thách thức ghê gớm của sự phát triển vắc-xin sốt Lass là yêu cầu phát triển cơ chế bảo vệ chủ yếu qua trung gian tế bào T, vì các phản ứng tế bào T CD4 + bộ nhớ mạnh đối với LASV NP và GP2 của các chủng LASV khác nhau đã được chứng minh ở một số người sống sót Nhiễm LASV ở Guinea ( 368 , 369 ). Điều này phù hợp với các quan sát rằng, trong khi các tế bào T CD4 có thể bảo vệ một phần động vật được tiêm vắc-xin ML29 trước thách thức LASV gây chết người, làm cạn kiệt tế bào T CD8 + hủy bỏ hoàn toàn sự bảo vệ ( 370 ). Ngoài ra, các tế bào T CD8 đặc hiệu NP đóng vai trò bảo vệ chính ở những con chuột bị nhiễm LCMV ( 279 ).
Ngoài việc phát triển vắc-xin như một biện pháp phòng ngừa, việc phát hiện ra các loại thuốc chống vi-rút là một lĩnh vực đang phát triển của nghiên cứu arenavirus. Hiện nay, phương pháp điều trị chống vi-rút duy nhất đang được sử dụng trên lâm sàng dành riêng cho mammarenaviruses là liệu pháp huyết tương điều trị chống lại JUNV ( 175 ). Các chất tương tự nucleoside chống virus tiêu chuẩn, chẳng hạn như Ribavirin và Favipiravir ( 69 , 371 - 374 ) đã thấy thành công lâm sàng vừa phải, nhưng chỉ hiệu quả khi được sử dụng trong giai đoạn sớm nhất của nhiễm trùng khi các triệu chứng chủ yếu là không đặc hiệu ( 173 ). Các oligomers morpholino liên hợp peptide cũng đã được thử nghiệm như các chất tương tự nucleoside thay thế, làm giảm các chuẩn độ của một số arenavirus trong nuôi cấy tế bào và chuột bị nhiễm LCMV (375 ). Tuy nhiên, sự phục hồi đã được ghi nhận bằng quản lý triệu chứng thay cho các chất tương tự nucleoside do sự chậm trễ trong chẩn đoán đạt được sau khi giải quyết các triệu chứng ( 376 ), hạn chế mong muốn sử dụng các chất tương tự nucleoside làm hợp chất chống virut.
Những tiến bộ gần đây trong phát hiện thuốc chống vi-rút đã tập trung vào việc xác định các hợp chất đặc biệt nhắm mục tiêu protein virut hoặc điều chỉnh hoạt động của protein chủ ( 377 ). Phần lớn phát hiện thuốc arenavirus đã tập trung vào các chất ức chế phân tử nhỏ của glycoprotein mammarenavirus và sự xâm nhập tế bào, đã thấy một số thành công với một số cách tiếp cận khác nhau. Các polyme DNA lưỡng tính đã được tìm thấy để ngăn chặn tương tác LCMV GP-α-dystroglycan nhờ vào tính kỵ nước của nó chứ không phải là trình tự nucleotide ( 378 ). Các dẫn xuất Clotrimazole, theo truyền thống nhắm vào kênh kali kích hoạt canxi KCa3.1, gần đây cũng đã được tìm thấy để ức chế phản ứng tổng hợp màng arenavirus ( 379). Tuy nhiên, cơ chế hoạt động của nó được phát hiện là độc lập với KCa3.1, và do đó hiện chưa rõ ràng.
Ngược lại, một số hợp chất khác đã được tìm thấy để ổn định sự hình thành phức hợp tiền xử lý GP-a-dystroglycan, do đó ngăn chặn endocytosis qua trung gian pH ( 380 - 384 ). Một trong những hợp chất này (ST-193) đã được tìm thấy để làm giảm chuẩn độ LASV trong mô hình nhiễm chuột lang ( 385 ). Một phân tử nhỏ khác (LHF-535) gần đây đã được tìm thấy có tác dụng ức chế nhiều loại arenavirus ngoại trừ các chủng có đột biến V434I, tương ứng với đột biến chịu trách nhiệm về sự suy giảm ở Candid # 1, cho thấy rằng nó cũng có thể ảnh hưởng đến ổn định tiền phức tạp ( 386 ). Cuối cùng, người ta cũng chứng minh rằng một chất ức chế phân tử nhỏ của protease vị trí tế bào 1 (PF-429292) có thể ngăn chặn quá trình xử lý GP ( 387, 388 ) cũng như có thể đóng vai trò là thuốc kháng vi-rút nói chung bằng cách ức chế tổng hợp lipid và cholesterol cần thiết cho sự nhân lên của vi-rút ( 389 - 392 ).
Một số hợp chất dược phẩm cũng đã được tìm thấy để phá vỡ các chức năng bình thường của protein mammarenavirus. Cho rằng myristoylation là cần thiết cho arenavirus qua trung gian Z ( 160 , 161 ), các hợp chất ức chế enzyme myristoylation ( 161 , 393 ) đã được tìm thấy để thay đổi nội địa hóa tế bào của Z và do đó ức chế virion nảy mầm từ các tế bào bị nhiễm bệnh. Các hợp chất thơm nhắm vào họa tiết ngón tay kẽm của Z cũng đã được tìm thấy để ức chế sự tăng sinh arenavirus ( 394 , 395). Một loạt các hiệu ứng cơ học đã được đặc trưng cho một trong những hợp chất này. Ví dụ, hợp chất NSC20625 đã được tìm thấy để tạo ra Z để mở ra và tích lũy trong các cấu trúc oligomeric ( 394 ) và do đó ngăn chặn sự tương tác của Z với protein PML chủ và cho phép các cơ thể hạt nhân hình thành ( 396 ). Các arenavirus L polymerase và NP được cho là có ít tiến triển nhất là các mục tiêu ma túy. Đối với trường hợp trước đây, một mục tiêu dược phẩm tiềm năng hấp dẫn là cơ chế giật nắp của polymerase arenavirus. Một loại thuốc tương tự đã được chứng minh là làm giảm chuẩn độ của virus West Nile ( 397 ). Tính đặc hiệu của cơ chế giật nắp virus ( 398) và sự nghi ngờ rằng các cơ chế giật nắp của arenavirus có thể được bảo tồn giữa các loài ( 399 , 400 ) khiến cho việc chụp mũ trở thành mục tiêu điều trị đầy hứa hẹn cho sự phát triển thuốc chống virut ( 401 ). Một số chất thải kim loại thực sự đã được tìm thấy có khả năng ức chế miền endonuclease LCMV và hoạt động giật nắp tiếp theo của nó, chứng tỏ tiềm năng cho các thuốc chống siêu vi trong tương lai nhắm vào tính năng virus này ( 404 ). Đột biến virus gây chết người cũng đã được xác định là một cơ chế có thể để kiểm soát virus ( 403 , 404). Trong khi một số nghiên cứu đã tìm thấy các loại thuốc nhắm vào các NP arenavirus, một bài báo gần đây đã xác định được một hợp chất từ thư viện pyridine có thể làm giảm sự chuẩn độ LCMV sau tế bào và được cho là ảnh hưởng đến NP và Z bởi các cơ chế chưa biết ( 405 ).
Các loại thuốc nhắm mục tiêu protein chủ cũng đang được khám phá như là liệu pháp dược phẩm tiềm năng. Genistein ức chế tyrosine kinase hiện là một trong những hợp chất được hỗ trợ nhiều nhất, vì sự phosphoryl hóa ATF-2 đã được tìm thấy là rất quan trọng đối với khả năng sống sót của PIC PICV, dễ bị genistein in vitro ( 406 , 407 ) và in vivo ( 408 ) . Các sàng lọc thuốc quy mô lớn hơn dường như cho thấy sự ức chế kinase của tế bào như là một mục tiêu chống vi-rút đầy hứa hẹn nói chung, với các hợp chất ảnh hưởng đến arenavirus ở nhiều giai đoạn của vòng đời vi-rút ( 409 - 411 ). Các chất ức chế sản xuất nucleoside cũng đã được thử nghiệm trong nhiều loại in vitro bối cảnh ( 412 - 414 ) và có thể có tác dụng phụ khi được sử dụng cùng với các chất tương tự nucleoside ( 412 ). Mặc dù các hợp chất này dường như không ảnh hưởng tiêu cực đến sức sống của nuôi cấy tế bào, chúng nên được khám phá một cách thận trọng do các tác động bất lợi có thể có trên một số tế bào đang phát triển nhanh chóng trên cơ thể . Cuối cùng, có thể nhắm mục tiêu các protein tín hiệu miễn dịch dưới dạng kiểm soát chống virut, với một chất ức chế chống TLR cho thấy hạn chế phản ứng cytokine do LCMV khởi tạo ở tế bào và sao chép virus ở chuột ( 294). Đối với tất cả các loại thuốc chống vi rút tiềm năng, tác dụng phụ nghiêm trọng (ví dụ, trong sự phát triển thần kinh và phôi thai) do độc tính tế bào đã biết của các hợp chất này có thể là một trở ngại lớn cho việc áp dụng rộng rãi các hợp chất này trong điều trị nhiễm arenavirus. Sự phát triển vắc-xin và thuốc chống vi-rút trong tương lai vẫn đang rất cần thiết để chống lại các mầm bệnh gây chết người này.
Tóm tắt và định hướng tương lai
Điều quan trọng là phải nhắc lại vai trò quan trọng của con đường IFN1 và khả năng miễn dịch qua trung gian tế bào T trong việc kiểm soát nhiễm trùng mammarenavirus ( 209 ). Những con đường này cũng được biết là rất quan trọng đối với cả đáp ứng miễn dịch bẩm sinh và đáp ứng miễn dịch đối với các mô hình nhiễm virus RNA khác ( 415 , 416 ) cũng như trong quá trình tiêm chủng ( 417 ), minh họa thêm tầm quan trọng cho các nghiên cứu trong tương lai của từng cơ chế này và trong buổi hòa nhạc. Ngoài ra, tiếp tục các nỗ lực sinh thái để mô tả đặc điểm phát sinh và lan truyền của arenavirus ( 2 , 9 , 18 , 21 , 46), các nỗ lực kinh tế xã hội để nâng cao nhận thức và khả năng ngăn chặn bệnh tật của công chúng ( 49 - 53 ), và cần có sự phát triển về vắc-xin và trị liệu để tối ưu hóa các biện pháp phòng ngừa và kiểm soát đối với mammarenaviruses.TINH THAT KIM LIEN .THICH NU CHAN TANH.AUSTRALIA,SYDNEY.4/8/2020.
No comments:
Post a Comment