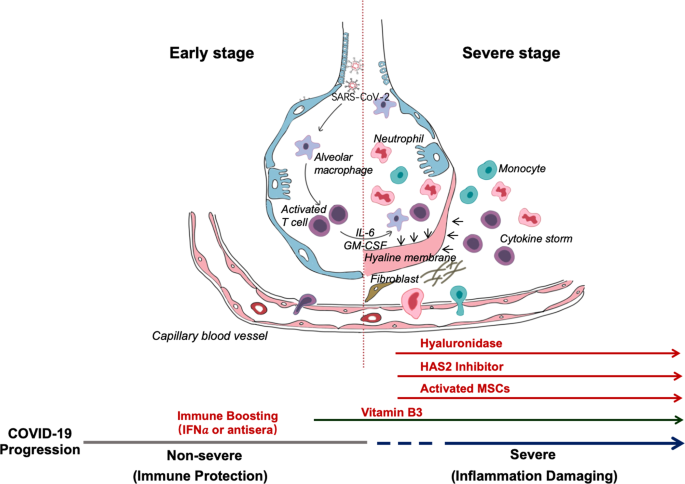
Phản ứng miễn dịch hai pha gây ra bởi nhiễm COVID-19.CHUYEN NGU TIENG ANH SANG TIENG VIET=THICH NU CHAN TANH.
Trên lâm sàng, các phản ứng miễn dịch gây ra bởi nhiễm SARS-CoV-2 là hai giai đoạn. Trong giai đoạn ủ bệnh và giai đoạn không nghiêm trọng, cần có đáp ứng miễn dịch thích nghi cụ thể để loại trừ virut và ngăn chặn sự tiến triển của bệnh đến giai đoạn nghiêm trọng. Do đó, các chiến lược để tăng cường đáp ứng miễn dịch (chống huyết thanh hoặc pegylated IFNα) ở giai đoạn này chắc chắn rất quan trọng. Để phát triển đáp ứng miễn dịch bảo vệ nội sinh ở giai đoạn ủ bệnh và giai đoạn không nghiêm trọng, vật chủ phải có sức khỏe tốt và nền tảng di truyền thích hợp (ví dụ: HLA) có khả năng miễn dịch chống vi rút cụ thể. Sự khác biệt di truyền được biết đến để đóng góp vào các biến thể cá nhân trong phản ứng miễn dịch với mầm bệnh. Tuy nhiên, khi đáp ứng miễn dịch bảo vệ bị suy giảm, virus sẽ lan truyền và sự phá hủy lớn các mô bị ảnh hưởng sẽ xảy ra, đặc biệt là trong các cơ quan có biểu hiện ACE2 cao, chẳng hạn như ruột và thận. Các tế bào bị tổn thương gây ra viêm bẩm sinh trong phổi mà phần lớn là trung gian bởi các đại thực bào viêm và bạch cầu hạt. Viêm phổi là nguyên nhân chính của rối loạn hô hấp đe dọa tính mạng ở giai đoạn nghiêm trọng [4 ]. Do đó, sức khỏe tổng quát tốt có thể không có lợi cho những bệnh nhân đã chuyển sang giai đoạn nghiêm trọng: một khi tổn thương phổi nghiêm trọng xảy ra, cần nỗ lực để ngăn chặn tình trạng viêm và kiểm soát các triệu chứng.
Đáng báo động, sau khi xuất viện, một số bệnh nhân vẫn còn / trở lại dương tính với virus và những người khác thậm chí tái phát. Điều này chỉ ra rằng đáp ứng miễn dịch loại bỏ virus đối với SARS-CoV-2 có thể khó gây ra ít nhất ở một số bệnh nhân và vắc-xin có thể không hoạt động ở những người này. Những người được phục hồi từ giai đoạn không nghiêm trọng nên được theo dõi vi-rút cùng với phản ứng của tế bào T / B. Những kịch bản này cần được xem xét khi xác định các chiến lược phát triển vắc-xin. Ngoài ra, có nhiều loại hoặc phân nhóm của coronavirus. Do đó, nếu vắc-xin nhắm trực tiếp vào SARS-CoV-2 tỏ ra khó phát triển, nên xem xét phương pháp Edward Jenner.
Cơn bão Cytokine và tổn thương phổi
Hội chứng giải phóng cytokine (CRS) dường như ảnh hưởng đến những bệnh nhân mắc bệnh nặng. Vì giảm bạch cầu lympho thường thấy ở bệnh nhân COVID-19 nặng, CRS gây ra bởi virus SARS-CoV-2 phải qua trung gian bởi bạch cầu khác với tế bào T, như ở bệnh nhân đang điều trị bằng CAR-T; số lượng WBC cao là phổ biến, cho thấy nó, liên quan đến giảm bạch cầu lympho, như là một tiêu chí chẩn đoán phân biệt cho COVID-19. Trong mọi trường hợp, chặn IL-6 có thể có hiệu quả. Chặn IL-1 và TNF cũng có thể có lợi cho bệnh nhân. Mặc dù các địa điểm lâm sàng khác nhau ở Trung Quốc đã công bố việc sử dụng tế bào gốc / tế bào gốc trung mô (MSC) trong các trường hợp nặng bị nhiễm COVID-19, nhưng vẫn chưa thấy kết quả chắc chắn. Một lưu ý là các MSC cần được kích hoạt bằng IFNγ để phát huy tác dụng chống viêm của chúng, có thể vắng mặt ở những bệnh nhân bị ảnh hưởng nghiêm trọng vì các tế bào T không được kích hoạt tốt do nhiễm SARS-CoV-2. Để nâng cao hiệu quả, người ta có thể cân nhắc sử dụng dịch vụcấp phép tiếp cận trực tiếp : các tiền xử lý MSC với IFNγ có / không có TNF hoặc IL-1 [ 5 ]. Các MSC được cấp phép cytokine này có thể có hiệu quả hơn trong việc ức chế đáp ứng miễn dịch siêu hoạt động và thúc đẩy sửa chữa mô, vì các MSC được cấp phép có hiệu quả trong tổn thương phổi cấp do LPS gây ra [ 6 ].
Tổn thương phổi là một trở ngại lớn cho sự phục hồi ở những bệnh nhân nặng. Thông qua việc tạo ra các yếu tố tăng trưởng khác nhau, MSC có thể giúp sửa chữa các mô phổi bị tổn thương. Điều quan trọng cần đề cập là các nghiên cứu khác nhau đã chỉ ra rằng trong các mô hình động vật bị tổn thương phổi do bleomycin, vitamin B3 (niacin hoặc nicotinamide) có hiệu quả cao trong việc ngăn ngừa tổn thương mô phổi [ 7 ]. Nó có thể là một cách tiếp cận khôn ngoan để cung cấp thực phẩm bổ sung này cho bệnh nhân COVID-19.
Haplotypes và nhiễm SARS-CoV-2
Các locus kháng nguyên phức hợp tương hợp mô học chính (HLA) là những ứng cử viên nguyên mẫu cho tính nhạy cảm di truyền đối với các bệnh truyền nhiễm [ 8 , 9 ]. Biến đổi Haplotype HLA-loci là kết quả của áp lực chọn lọc trong quá trình đồng tiến hóa với mầm bệnh. Các nhà miễn dịch học đã tìm thấy các thụ thể kháng nguyên tế bào T, trên CD4 + hoặc CD8 + Các tế bào T nhận ra cấu trúc hình dạng của liên kết kháng nguyên-kháng nguyên cùng với các peptide kháng nguyên liên quan. Do đó, các haplotypes khác nhau có liên quan đến tính nhạy cảm bệnh khác nhau. Các tiết mục của các phân tử HLA tạo thành một haplotype quyết định sự sống còn trong quá trình tiến hóa. Theo đó, có vẻ thuận lợi khi có các phân tử HLA với độ đặc hiệu liên kết tăng với các peptide virus SARS-CoV-2 trên bề mặt tế bào của các tế bào trình diện kháng nguyên. Thật vậy, tính mẫn cảm với các bệnh truyền nhiễm khác nhau như bệnh lao, bệnh phong, HIV, viêm gan B và cúm có liên quan đến các haplotypes cụ thể của HLA. Haplotypes Murine loại II đặc biệt có liên quan đến sự nhạy cảm với bệnh cúm. Ở nam giới, lớp HLA I cũng có liên quan đến nhiễm trùng H1N1: HLA-A * 11, HLA-B * 35,10 ]. Do đó, cần phải nghiên cứu xem các locus HLA cụ thể có liên quan đến sự phát triển của miễn dịch chống SARS-CoV-2 hay không, và nếu vậy, để xác định các alen, loại I hoặc II, chứng tỏ khả năng miễn dịch bảo vệ. Khi các alen trội được xác định, các bộ phát hiện đơn giản có thể được phát triển. Những thông tin này rất quan trọng đối với (1) quản lý lâm sàng chiến lược; (2) đánh giá hiệu quả của việc tiêm phòng ở những người khác nhau trong dân số nói chung; (3) phân công đội ngũ quản lý và chuyên môn lâm sàng trong bối cảnh tương tác với bệnh nhân COVID-19.
Hyaluronan: một nguyên nhân gây tử vong
Phản ứng miễn dịch bẩm sinh đối với tổn thương mô do virus gây ra có thể dẫn đến hội chứng suy hô hấp cấp tính (ARDS), trong đó suy hô hấp được đặc trưng bởi sự khởi phát nhanh chóng của viêm lan rộng trong phổi và tử vong sau đó [ 4 ]. Các triệu chứng của bệnh nhân ARDS bao gồm thở ngắn / nhanh và tím tái. Bệnh nhân nặng được đưa vào các đơn vị chăm sóc đặc biệt thường yêu cầu máy thở cơ học và những người không thể thở được phải được kết nối với oxy hóa màng ngoại bào (ECMO) để hỗ trợ sự sống [ 11 ]. Hình ảnh CT tiết lộ rằng có những mảng trắng đặc trưng gọi là kính mặt đất , có chứa chất lỏng trong phổi [ 2]. Các khám nghiệm tử thi gần đây đã xác nhận rằng phổi chứa đầy chất lỏng trong suốt, giống như phổi của đuối nước ướt [ 4 ]. Mặc dù bản chất của thạch rõ ràng vẫn chưa được xác định, hyaluronan (HA) có liên quan đến ARDS [ 12 ]; hơn nữa, trong quá trình nhiễm SARS, việc sản xuất và điều tiết hyaluronan bị khiếm khuyết. Mức cytokine viêm (IL-1, TNF) là cao trong phổi của COVID-19 bệnh nhân và những cytokine là thuốc gây cảm ứng mạnh mẽ của HA-synthase-2 (HAS2) trong CD31 + nội mạc, EpCAM + phổi phế nang tế bào biểu mô, và nguyên bào sợi [ 13]. Điều quan trọng, HA có khả năng hấp thụ nước gấp 1000 lần trọng lượng phân tử của nó. Do đó, việc giảm sự hiện diện hoặc ức chế sản xuất HA giữ một lời hứa lớn trong việc giúp bệnh nhân COVID-19 thở. Các bác sĩ có thể chỉ cần cung cấp cho bệnh nhân hyaluronidase cấp y tế để giảm sự tích tụ HA và do đó để làm sạch thạch trong phổi. Trong các mô hình động vật, khó thở do cúm có thể được làm dịu bằng cách sử dụng hyaluronidase nội sọ. Các bác sĩ cũng có thể sử dụng một loại thuốc trị liệu mật được phê duyệt lâm sàng, Hymecromone (4-Methylumbelliferone, 4-MU), một chất ức chế HAS2 [ 14]. Viêm phổi do LPS gây ra có thể thuyên giảm bằng 4-MU. 4-MU hoặc các dẫn xuất hóa học của nó tồn tại rộng rãi trong các loại thảo mộc khác nhau được sử dụng trong y học cổ truyền Trung Quốc, điều này có thể giải thích hiệu quả quan sát được của thuốc thảo dược kết hợp ở một số bệnh nhân.
Nhìn chung, tóm tắt này dựa trên một số ý nghĩa chung về lâm sàng. Chúng tôi đề xuất một số cách tiếp cận đơn giản, nhưng phần lớn bị bỏ qua, trong điều trị bệnh nhân COVID-19 (Hình 1). Chúng tôi tin rằng sự phân chia hai pha là rất quan trọng: giai đoạn bảo vệ dựa trên hệ thống phòng thủ miễn dịch đầu tiên và giai đoạn gây tổn thương do viêm nhiễm thứ hai. Các bác sĩ nên cố gắng tăng cường đáp ứng miễn dịch trong lần đầu tiên, đồng thời ức chế nó trong giai đoạn thứ hai. Vì Vitamin B3 có tính bảo vệ phổi cao, nên được sử dụng ngay khi bắt đầu ho. Khi khó thở trở nên rõ ràng, hyaluronidase có thể được sử dụng trong khí quản và đồng thời có thể dùng 4-MU để ức chế HAS2. Tất nhiên, gõ HLA sẽ cung cấp thông tin nhạy cảm để chiến lược phòng ngừa, điều trị, tiêm phòng và phương pháp lâm sàng. Chúng tôi hy vọng rằng một số ý tưởng trên có thể được sử dụng để giúp chống lại căn bệnh truyền nhiễm chết người này với tỷ lệ mắc ngày càng tăng trên toàn thế giới.
Sau một thời gian ủ bệnh, virus COVID-19 xâm nhập gây ra các triệu chứng không nghiêm trọng và tạo ra các phản ứng miễn dịch bảo vệ. Việc loại bỏ thành công nhiễm trùng phụ thuộc vào tình trạng sức khỏe và haplotype của cá nhân bị nhiễm bệnh. Trong giai đoạn này, các chiến lược để tăng cường đáp ứng miễn dịch có thể được áp dụng. Nếu tình trạng sức khỏe chung và haplotype của cá nhân bị nhiễm bệnh không loại trừ được virus, thì bệnh nhân sẽ bước vào giai đoạn nghiêm trọng, khi xảy ra phản ứng viêm gây tổn thương mạnh, đặc biệt là ở phổi. Ở giai đoạn này, có thể kê đơn ức chế hyaluronan synthase và loại bỏ hyaluronan. Tế bào gốc trung mô hoạt hóa Cytokine có thể được sử dụng để ngăn chặn viêm và thúc đẩy tái tạo mô. Vitamin B3 có thể được cung cấp cho bệnh nhân bắt đầu có bất thường hình ảnh CT phổi.HET=TINH THAT KIM LIEN.THICH NU CHAN TANH.AUSTRALIA,SYDNEY.16/4/2020.
No comments:
Post a Comment